Evaluación de la
estabilidad de cápsulas de jugo de naranja obtenidas mediante gelificación iónica
Evaluation
of the stability of orange juice capsules obtained by ionic gelation
Juan Francisco
Castañón-Rodríguez, Maricela Guadalupe Soto-Gómez, Rocío Margarita
Uresti-Marín*
*Correspondencia:
ruresti@docentes.uat.edu.mx/Fecha de recepción: 12 de abril de 2019/Fecha de aceptación: 11 de diciembre de 2019/Fecha de publicación: 31 de enero de 2020.
Universidad
Autónoma de Tamaulipas, Unidad Académica de Trabajo Social y Ciencias para el
Desarrollo Humano, Centro Universitario, Cd. Victoria, Tamaulipas, México, C.
P. 87149.
Resumen
El método de gelificación iónica, como técnica
de encapsulación, se basa en las interacciones entre hidrocoloides,
las cuales previenen la posibilidad de daño de compuestos bioactivos
presentes en alimentos, tales como los jugos de cítricos. El objetivo del
presente estudio fue evaluar la estabilidad de las cápsulas de jugo de naranja,
obtenidas mediante gelificación iónica, utilizando
pectina y alginato de sodio como agentes encapsulantes. Se determinaron la pérdida de peso,
atributos de color, diámetro, morfología macroscópica y densidad en cápsulas elaboradas.
Se utilizó un diseño factorial, modificando la concentración de pectina de alto
metoxilo (1.5 %, 2 % y 2.5 % p/v), pH (2.5, 3.5 y
4.5) y sólidos solubles totales (SST) a 5 ºBrix y 15 ºBrix, manteniendo constante la concentración de alginato de sodio al 0.5 % (p/v), y se almacenaron a
temperatura ambiente (26 ºC) y refrigeración (4 ºC) durante 12 d. Las cápsulas presentaron principalmente
forma esférica (> 45 %). Los atributos de color
permanecieron estables durante 12 d de
almacenamiento. Los SST iniciales y el pH influyeron en la estabilidad de las
cápsulas. A una concentración de 15 ºBrix y pH 2.5 no
se pudieron formar de manera adecuada las cápsulas, presentando mayor sinéresis
y morfologías amorfas. Las cápsulas de jugo de naranja con concentración de
pectina 2 % (p/v), alginato de sodio 0.5 %
(p/v), SST 5 ºBrix
y pH 2.5, se mantuvieron estables con parámetros de calidad apropiados al ser
almacenadas a temperatura de refrigeración (4 ºC). El
método de gelificación iónica mediante encapsulación
ofrece una alternativa para prolongar la vida útil del jugo, y el desarrollo de
nuevos productos elaborados a partir de este cítrico.
Palabras clave: jugo de naranja, encapsulación, gelificación iónica, alginato de
sodio, pectina.
Abstract
The ionic gelation method as an encapsulation
technique is based on the interactions between hydrocolloids, which prevent the
possibility of damage of bioactive compounds present in foods, such as citrus
juice. Therefore, the objective of the present study was to evaluate the
stability of the orange juice capsules obtained by ionic gelation using pectin
and sodium alginate as encapsulating agents. The effects of the gelling agents
on the stability were determined by the measurement of weight loss,
diameter, color attributes, diameter,
macroscopic morphology, density in elaborate
capsules. In addition, a factor analysis design was used by modifying the
concentration of high methoxyl pectin (1.5 %, 2 % and
2.5 % w/v), pH (2.5, 3.5 and 4.5) and total soluble solids (TSS) at 5 ºBrix and
15 ºBrix, maintaining the concentration of sodium alginate constant at
0.5 % (w/v). The capsules were stored at
room temperature (26 ºC) and refrigeration (4 ºC) for 12 d. They mainly presented
a spherical shape (> 45 %). The color attributes remained stable even after
12 d of storage. The initial TSS and pH influenced the stability of the capsules. At a concentration of 15 ºBrix and pH 2.5, the capsules could not be adequately
formed, capsules presenting greater syneresis and amorphous morphologies. However, the
orange juice capsules remained stable for more than 2 weeks and with stable
quality parameters when stored at refrigeration
temperature (4 ºC), pectin concentration 2 % (w/v), sodium alginate 0.5
% (w/v), TTS 15 ºBrix and pH 2.5. The ionic gelation method through
encapsulation offers an alternative to extend the shelf life of the juice and the development of new products
made from this citrus.
Keywords: orange juice, encapsulation, ionic
gelation, sodium alginate, pectin.
Introducción
La encapsulación
es un proceso para atrapar agentes activos dentro de un material portador y es una herramienta útil para
mejorar la liberación de moléculas bioactivas y
células vivas en alimentos, ya que puede proporcionar barreras entre los materiales
bioactivos sensibles y el medio ambiente, así como
permitir la diferenciación de sabor y aroma, enmascarar malos sabores u olores,
evitar la evaporación y degradación de
compuestos volátiles que proporcionan aroma, prevenir reacciones con
otros componentes en productos alimentarios
como el oxígeno o el agua, estabilizar ingredientes alimentarios en
productos finales y durante el procesado o aumentar su biodisponibilidad y para
inmovilización de células o en zimas en aplicaciones
de procesamiento de alimentos, como procesos de fermentación y metabolitos,
industrias farmacéuticas (Gouin, 2004; Nedovic y col., 2011; Peanparkdee
y col., 2016).
Los
materiales utilizados para el diseño de la capa protectora de encapsulados
deben ser de calidad alimentaria, biodegradable y capaz de formar una barrera
entre la fase interna y su entorno. Entre todos los materiales, los más
utilizados para la encapsulación en aplicaciones alimentarias son las proteínas,
lípidos y polisacáridos; dentro de los polisacáridos más utilizados destacan
exudados y extractos vegetales, como la pectina, y extractos marinos, como alginatos (Nedovic y col., 2011).
Los alginatos son uno de los polímeros más utilizados
en la microencapsulación, estos compuestos son
extraídos primariamente de tres especies de algas marrones y son una familia de
polisacáridos lineales no ramificados, conteniendo cantidades variables de
ácido (1,4’) b-D-manurónico (M) y de ácido a-L-gulurónico
(G). Está compuesto por secuencias de residuos M (bloques M) y G (bloques G)
intercalados con secuencias MG (Bloques MG). La composición y extensión de las
secuencias y el peso molecular determinan las
propiedades físicas de los alginatos (Lupo y col., 2012).
Las perlas de alginato se han usado ampliamente en microencapsulación
porque son extremadamente fáciles de preparar a escala de laboratorio, el proceso es muy ligero, puede
ser realizado en ambientes estériles y prácticamente cualquier ingrediente
puede ser encapsulado, ya sea hidrófobo o hidrófilo, sensible a la temperatura,
un delgado líquido, un aceite viscoso, un sólido, etc. (Gouin,
2004). Dada su biocompatiblidad, biodegradabilidad y
propiedades de no toxicidad e inmunogénicas lo han hecho ser evaluado
como un biomaterial para la regeneración
tisular ósea (Venkatesan
y col., 2015), atrapamiento celular terapéutico o inmovilización celular, propiedades
inmunogénicas del alginato,
modificador de la red de polímeros de mucina, modificadores de la mucosidad en
fibrosis quística (Draget y Taylor, 2011) y la
posibilidad de atrapar diferentes tipos de células a través de ingeniería
celular y producir biomoléculas terapéuticas ha dado lugar a numerosas aplicaciones
novedosas (Orive y col., 2015).
Un método de
encapsulamiento es la gelificación iónica también
conocida como gelificación externa o ionotrópica, que se desarrolló inicialmente para la
inmovilización de células y el alginato es utilizado
principalmente como componente de la membrana y se utiliza la combinación de
calcio y bario (iones divalentes) para dar pie a la gelificación.
La aplicación más atractiva del alginato es la gelificación inducida por calcio, resultando en interacciones
específicas y fuertes entre los iones de calcio y residuos de guluronatos presentes en el alginato.
El tamaño de las partículas no puede ser bien controlado y las partículas
tienden a coagularse en grandes masas antes de adquirir la consistencia apropiada,
obteniendo partículas de tamaño, entre 400 mm y 1 mm (Krasae-koopt y col., 2003; Agulhon y col., 2014; San-doval y col., 2016), sin embargo, no ha sido utilizada la
pectina como agente encapsulante.
Los
polisacáridos pécticos o pectinas tienen una estructura
química extremadamente diversa, pero
comparten algunas características comunes, particularmente la presencia de ácido galacturónico y
generalmente son tres tipos de polisacáridos reconocidos como: homogalacturonanos (HG), ramnogalacturonano-I (RG I) y ramnogalacturonano-II (RG
II) (Willats y col., 2006). Las pectinas constituyen
alrededor del 35 % (p/p) de las paredes celulares primarias de las dicotiledóneas y monocotiledóneas no gramíneas (Willats y col., 2006; Mohnen,
2008) y presentan propiedades espesantes, estabilizantes y gelificantes, además de brindar estabilidad y viscosidad,
por su función emulsificante en combinación con
aceites comestibles da lugar a la producción de aceites esenciales empleados en
la producción de sabores. Los recubrimientos de pectina son utilizados debido a
sus propiedades mecánicas de adherencia y flexibilidad en la superficie (García
y col., 2004). Este polisacárido está atrayendo una mayor atención por los
efectos de salud prometedores que ha mostrado, tales como la disminución de los
niveles de colesterol, disminución de la glucemia y actividad anticancerígena (Liu y col., 2016).
Por otro
lado, las especies de cítricos son fuente ricas de vitamina C, folato, fibra
dietética y minerales además de muchos fitoquímicos,
incluyendo flavonoides, aminoácidos, triterpenos,
ácidos fenólicos y carotenoides (Li-Ying y col., 2008). Entre los productos de
frutas, destaca el jugo de naranja, como una fuente de flavanonas
en la dieta, principalmente hesperidina y narirutina. La naranja es uno de los frutos más populares y
consumidos en México por sus cualidades refrescantes y su sabor característico
ácido o dulce dependiendo de la variedad. México se consolidó como el quinto
productor mundial de naranja, con un volumen promedio
de 4.2 millones de T, las cuáles se comercializaron tanto en el mercado
como en destinos internacionales. Las principales
entidades productoras de este cítrico
son Veracruz, quien aporta el 44.5 % del volumen nacional; Tamaulipas
14.6 %, y San Luis Potosí 8.8 % de acuerdo a la Secretaría de Agricultura y Desarrollo Rural (SAGARPA, 2015).
La naranja
normalmente se consume como fruto fresco, sus subproductos se utilizan en la elaboración
de jarabes, jugos, refrescos, postres,
helados y pasteles. La oferta que la agroindustria mexicana procesadora
de jugos cítricos actualmente es de prácticamente 90 000 T de jugo concentrado
de naranja. Considerando únicamente a la agroindustria ubicada en la zona
citrícola que circunda al golfo de México (Veracruz, Nuevo León, Tamaulipas,
San Luis Potosí y Tabasco) y parte de la Península de Yucatán (Licona, 2009).
El jugo concentrado de naranja es el de mayor importancia en el mundo, tanto
por el volumen que se produce como por el
número de mercados que lo consumen, los principales centros de consumo
de jugo de naranja se ubican en Europa y Norteamérica (Licona, 2009). Sin embargo,
una de las principales desventajas del jugo de naranja natural, es su vida útil
corta por su alto contenido de azúcares, que si no se almacena bajo condiciones
adecuadas de temperatura comienza a degradarse y presentarse sabores
indeseables.
El objetivo del presente trabajo fue evaluar la estabilidad de las
cápsulas del jugo de naranja, utilizando como método de encapsulación la gelificación iónica, y usando pectina y alginato
de sodio como agentes encapsulantes bajo dos condiciones de
almacenamiento, a temperatura ambiente (26 ºC) y
refrigeración (4 ºC).
MATERIALES Y MÉTODOS
Materiales
Las
naranjas dulces (Citrus sinensis L. Osbeck) variedad Valencia fueron obtenidas de mercados de
Ciudad Victoria, Tamaulipas, las cuales fueron lavadas y desinfectadas, previamente
a la extracción del jugo. La pectina de alto metoxilo
(PAM) y alginato de sodio (AS) se obtuvieron de un proveedor
nacional (Quial comerciales, S.A. Tepic, México). Métodos
Gelificación iónica
Para la elaboración de las cápsulas utilizando gelificación iónica,
se utilizó el jugo de naranja recién extraído y filtrado, a 5 ºBrix y a 15 ºBrix (este se tomó
como referencia a la concentración del jugo natural que se determinó durante su caracterización).
Para la
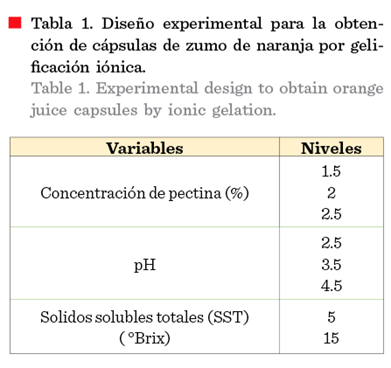
obtención de cápsulas mediante gelificación iónica se
utilizó un diseño factorial como se muestra en la Tabla 1, en el cual se
disolvieron diferentes concentraciones de
pectina de alto metoxilo (1.5 %, 2 % y 2.5 % p/v),
se modificó el pH (2.5, 3.5 y 4.5) y se ajustó el jugo a dos concentraciones de
sólidos solubles totales (SST) a 5 ºBrix y 15 ºBrix con ácido
cítrico y sacarosa; manteniendo constante la concentración de alginato de sodio al 0.5 % (p/v) el cual fue previamente
disuelto en el jugo, por otra parte se elaboró una disolución de lactato de calcio (Quial, México)
al 3 % (p/v).
Una vez obtenidas
ambas soluciones (alginato de sodio y lactato de
calcio), se procedió a verter gotas de la solución de alginato,
pectina y jugo, por medio de una piseta, sobre la
solución de lactato de calcio. Las cápsulas formadas se enjuagaron con agua destilada,
se separaron y almacenaron en recipientes de polipropileno de 10 mL con tapa y estériles, bajo dos condiciones de almacenamiento,
temperatura ambiente (26 ºC) a una HR 6 % y
refrigeración (4 ºC) a una HR de 85 %; ambas
condiciones (temperatura y humedad relativa) medidas mediante un termohigrómetro análogo A600FC, durante 12 d, realizando la medición de los siguientes parámetros cada 3 d.
Caracterización del zumo de naranja encapsulado con gelificación iónica
Peso
Las
cápsulas se colocaron en conjunto con su recipiente en la balanza analítica
(VELABTM, VE-210, Velab Co, USA), una vez obtenido este
peso se procedió a obtener el peso real de las cápsulas mediante diferencia con
el peso inicial. Para ello, se tomaban 5 cápsulas que se pesaban cada 3 d, y de
esta manera se determinaba la pérdida de peso.
Atributos de color
El análisis
de color de las cápsulas obtenidas se realizó con un colorímetro MiniScan EZ 45/0 LAV
(MSEZ1342) (Reston, VA, USA), Hunter Associates Laboratory HunterLab, determinando
los atributos Luminosidad (L*), Saturación
o Cromaticidad (C*), Tono (H*)
utilizando
las Ecuaciones (1) y (2), además de la determinación del cambio de color (rE)
durante el
almacenamiento utilizando L*, a* y b* (Ecuación 3).
Croma (C*)
= ((a *)2 + (b *)2)1/2 (1)
H*a,b=
tan-1(b*/a*) (2)
rE = [(L*)2 + (a*)2+
(b*)2] (3)
Diámetro
Se determinó el diámetro promedio de las cápsulas utilizando una cinta métrica flexible (Lufkin),
midiendo el diámetro de 5 cápsulas de cada tratamiento.
Morfología
macroscópica
Se
colocaron 5 cápsulas sobre una caja Petri, con fondo blanco y buena
iluminación, mediante observación se determinó su morfología de manera visual,
además de observar los cambios y alteraciones que sucedieron durante los 12 d
de evaluación.
pH
El pH del jugo encapsulado que se obtuvo cada 3 d mediante la ruptura de las cápsulas, se
midió con un potenciómetro (Thermo Scientific, Orion Star A1210, Waltham, MA, USA) y
un electrodo (Hanna instruments)
previamente calibrado con solución reguladora de pH 4,
7 y 10 (JT Baker®, Modelos 5657-01, 5656-01, 5655-01, Edo. de México, México).
Densidad
Se utilizó
un método indirecto considerando que las cápsulas son de formas irregulares
entre sí,
se tomó una muestra de 5 esferas y se pesaron
en una balanza analítica (VELABTM, VE-210, Velab Co, USA) para obtener su masa. El volumen final se
obtuvo al sumergir en una probeta con 1 mL de agua destilada
(volumen inicial), la cual fue medida con una pipeta serológica, la densidad de
las cápsulas se calculó dividiendo la masa entre la diferencia del volumen
final y el volumen inicial.
Análisis estadístico
Se utilizó el programa de Excel (Microsoft Office 2010) para
la determinación de las medidas de tendencia central y realización de
gráficas, y el software Statistica 7.0 (StatSoft
Inc.,
Tulsa, OK, USA) para establecer diferencias entre tratamientos, empleando el método
de pruebas de rangos múltiples de Diferencias Mínimas Significativas (LSD, por
sus siglas en inglés: Least Significant
Difference) y las diferencias fueron consideradas
significativas cuando P ≤ 0.05.
RESULTADOS Y DISCUSIÓN
Parámetros fisicoquímicos del zumo de naranja en capsulado
con gelificación iónica En la Figura 1, se muestran los resultados de las
pérdidas de peso de las cápsulas obtenidas mediante gelificación
iónica a 5 ºBrix y 15 ºBrix
durante los 12 d de almacenamiento a temperatura ambiente (26 ºC) y refrigeración (4 ºC), en la
cual se aprecia que la pérdida de peso fue mayor en las cápsulas a 15 ºBrix, independientemente de las condiciones de
almacenamiento. No se muestran los resultados a 15 ºBrix,
a pH de 2.5, porque bajo ninguna concentración de pectina evaluada a este pH, y
esta concentración de SST, se formaron
cápsulas estables.
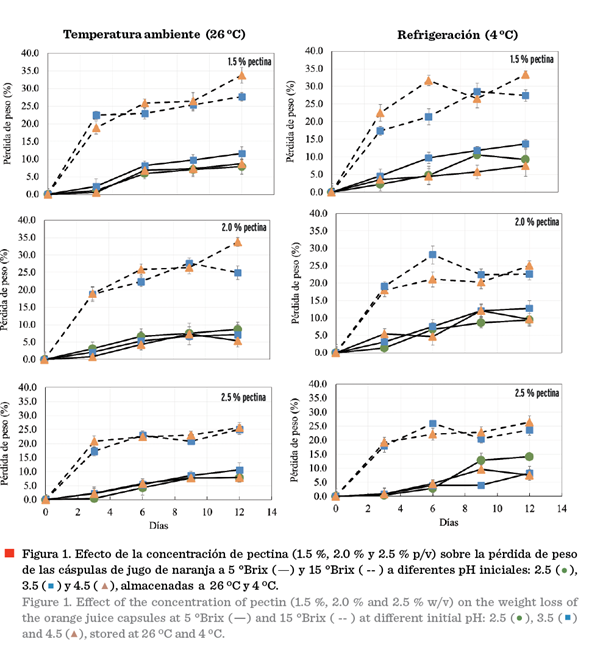
En las
cápsulas obtenidas con jugos con diferentes concentraciones de SST, la pérdida
de
peso más
notable fue al día 12, observándose la mayor pérdida de peso (34 %) en las
cápsulas de 15 ºBrix,
1.5 % pectina y pH 4.5 tanto a 26 ºC como 4 ºC. También se presentó el mismo porcentaje de pérdida de
peso en las cápsulas de 15 ºBrix 2.5 % de pectina, a 26 ºC.
Este comportamiento podría deberse a que quizá la pared del agente encapsulante sea tan delgada que provoque la salida del
jugo encapsulado por sinéresis. El agua liberada es evaporada de la superficie
de la cápsula por las corrientes de aire generadas en el interior
del refrigerador, con la consecuente pérdida
de peso. Cabe mencionar que hay interacciones en los hidrocoloides
utilizados y el agua, lo que influye en la evaporación o pérdida de la
misma en las cápsulas, que está determinada por parámetros moleculares de las
macromoléculas, propiedades del material a encapsular
y morfología de las partículas, además de condiciones externas, como
temperatura, humedad y pH, tal como lo
menciona Einhorn-Stoll (2018).
En las cápsulas
almacenadas a 4 ºC, a concentración de 2.0 % y 2.5 %
(p/v) no se observaron diferencias significativas (P ≤ 0.05) en la pérdida de peso (21 % a 25 %), independientemente
del pH evaluado.
Las cápsulas con concentración de 5 ºBrix, presentaron una disminución porcentual de peso menos notoria, oscilando de 5 % a 12 %, a 26 ºC, independientemente
de la concentración de pectina y pH evaluados. La mayor pérdida (12 %)
se obtuvo a pH 3.5. Las pérdidas fueron más
evidentes a 4 ºC, oscilando de 7 % a 14 % en las diferentes concentraciones de pectina.
El factor que más influyó en la pérdida de peso fue la concentración de SST,
puesto que las cápsulas en condición de almacenamiento a temperatura ambiente y
refrigeración con 15 ºBrix presentaron un porcentaje
de pérdida de peso mayor. Es de resaltar, que la mayor pérdida de peso con esta
concentración de SST ocurrió entre el día 0 al 3, para ambas condiciones de almacenamiento. Debido a que una cápsula
está conformada por una membrana
semipermeable, de forma esférica, paredes delgadas y fuertes, estas se encargan
de proteger el centro sólido/líquido, el agua del interior en combinación con
los sólidos disueltos en ella. Esa permeabilidad pudo haber influido en la modificación de este parámetro durante
el almacenamiento, ya que el proceso de encapsulamiento coadyuva a que los
compuestos bioactivos presentes en el producto alimenticio encapsulado resistan ciertas condiciones durante el procesamiento y empacado,
y proteja de degradación o transformación
física, química o enzimática, con la consecuente pérdida de bioactividad (Dias y col., 2015).
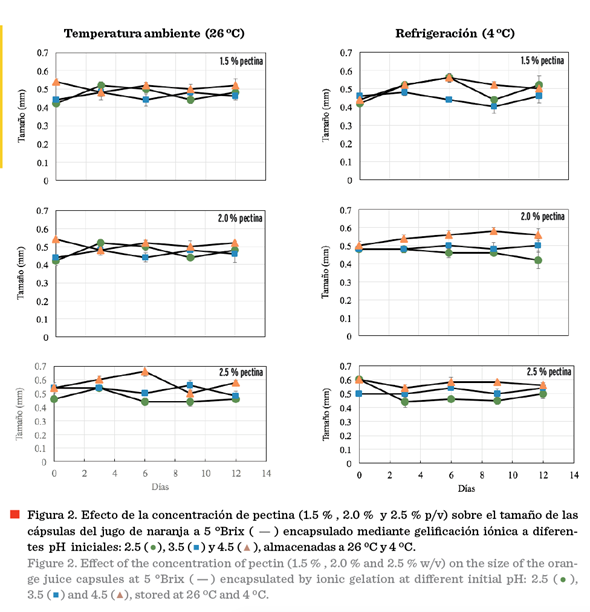
El tamaño
de las cápsulas de jugo de naranja, almacenadas a temperatura ambiente (26 ºC)
y refrigeración (4 ºC) a 5 ºBrix
se muestra en la Figura 2. El
diámetro osciló de 0.42 mm a 0.66 mm a 26 ºC, a las
diferentes concentraciones de pectina, siendo los tamaños mayores los obtenidos
con pH de 4.5, mientras que a los otros pH (2.5 y 3.5) no se observaron
diferencias significativas en el día 1; y a 4 ºC, los
tamaños de las cápsulas oscilaron de 0.41 mm
a 0.58 mm, con las diferentes concentraciones de pectina. Este atributo
no varió en las muestras con 1.5 % de pectina. Las cápsulas obtenidas a 2.0 % y
2.5 % de pectina presentaron los tamaños menores.
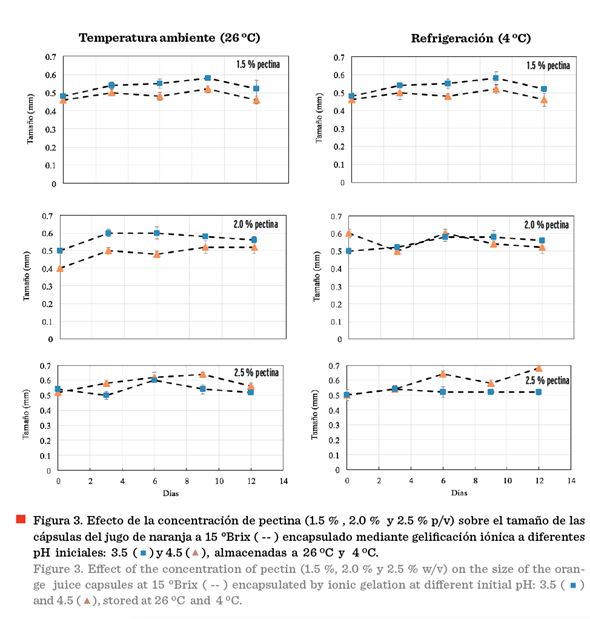
Las
cápsulas obtenidas a 15 ºBrix (Figura 3) variaron de
0.40 mm a 0.61 mm, almacenadas a 26 ºC. El tamaño de la cápsula almacenada a 4 ºC osciló de 0.46 mm a 0.68 mm en las diferentes
concentraciones de pectina y pH evaluados,
observándose los tamaños mayores a 2.5
% (p/v) de pectina y pH 4.5, mientras que a concentraciones de 1.5 % y 2.0
% (p/v) de pectina, las cápsulas de mayor tamaño fueron con un pH de 3.5.
De acuerdo
a Parra (2010), el tamaño de las cápsulas elaboradas con alginatos
no puede
ser del todo
controlado, pero normalmente oscila de 400 mm y a 1 mm, para su fácil deglución, una
vez que las cápsulas son sometidas a un secado posterior. En este estudio,
las cápsulas
no fueron sometidas a un proceso de secado posterior, es por ello su tamaño es
mayor. De acuerdo a Krasaekoopt y col. (2003), el tamaño de las esferas es de 2
mm a 5 mm y la forma de las cápsulas de alginato de sodio está determinado por el diámetro de la aguja usada y la
distancia de la caída libre de la solución. Además, esta morfología podría ser
debido a las interacciones de la pectina y el alginato
en geles mixtos, que se han descrito como una asociación heterogénea de los
bloques poli-G de alginato y éster metílico de las
regiones de pectina de baja carga,
empaquetadas en perlas rígidas (Voo y col.,
2011).
En la Tabla
2 se muestran los valores de la densidad de las cápsulas de jugo de naranja. En
la cápsula almacenada a 26 ºC la densidad inicial más baja (0.88 g/mL)
y más alta (2.30 g/mL) fue observada a 5 ºBrix, pH 4.5 y concentraciones de pectina de 2 % y 1.5
% (p/v), respectivamente, mientras que las
densidades finales a esta misma concentración de SST osciló de 0.63 g/mL a 1.04 g/mL. A 15 ºBrix, la densidad inicial obtuvo valores entre 1.11 g/mL y 2.03 g/mL. A concentración de 2 % (p/v) de pectina, pH 3.5
% se obtuvo la mayor densidad inicial. Las
densidades más bajas se obtuvieron a 2.5 % (p/v) de pectina con los pH
evaluados. La densidad inicial varió de 0.72 g/mL a
1.51 g/mL. Los cambios de densidad pueden ser debido a
que la pectina, muestra una menor sensibilidad a agentes químicos, en este
caso, al pH del jugo, además de una mayor resistencia mecánica en comparación con alginato (Naqash
y col., 2017). Es posible que se haya presentado un efecto sinérgico, al hacer
la combinación de ambos agentes encapsulantes que
influyeron en la densidad de las cápsulas.
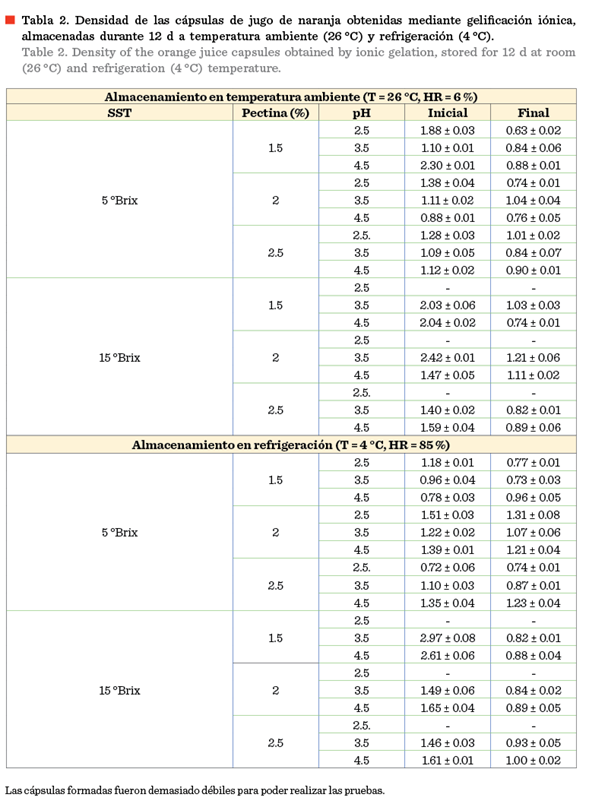
A 15 ºBrix, las cápsulas mostraron densidades más altas, cuyos valores oscilaron entre 1.46 g/mL y 2.97 g/mL. La densidad más alta se obtuvo a concentración de 1.5 % (p/v)
de pectina. De acuerdo a Rivera (2013), la
densidad de las esferas de alginato sufre cierta
influencia debido a la concentración en que se han elaborado y el tiempo de gelificación, sin
embargo, las cápsulas obtenidas mediante este método de encapsulamiento mostraron una apariencia y homogeneidad
en su tamaño y forma, a pesar de los
cambios de densidad que sufrieron
durante su almacenamiento.
El comportamiento
de los cambios que tuvo el pH de las cápsulas de naranja a 5 ºBrix y 15 ºBrix, en las cápsulas
almacenadas a 26 ºC y 4 ºC,
se muestra en la Figura 4. El pH inicial 3.5
y 4.5 tendió a disminuir en las muestras
almacenadas a temperatura ambiente,
alcanzando valores de 2 a 2.5 a los 12 d, en tanto que el pH 2.5 permaneció estable. En
temperatura de refrigeración el pH 3.5 y 4.5, presentó una disminución general para
el día 6, con un incremento al día 12, en las muestras con 2.5 % y 3.5 % de pectina.
En algunas cápsulas se observó cierta
sinéresis que pudo haber sido causada por estas modificaciones de pH, ya que al
inicio existió degradación de las cápsulas,
que se pudo apreciar de manera visual al momento de realizar las
determinaciones, pero no una desintegración total, a excepción del pH de 1.5, donde su formación fue más lenta y más
débil. Esta inestabilidad del pH pudo haber afectado la estabilidad de las
cápsulas, de acuerdo a lo reportado por Einhorn-Stoll
y col. (2015), ya que ocurren enlaces de hidrógeno
en los grupos carboxilo no disociados y no cargados a pH bajos, que favorecen
fuertes interacciones en las macromoléculas de la pectina de las cápsulas. En contraste,
los grupos carboxilo disociados a pH más altos están cargados negativamente y causa
repulsión electrostática de las macromoléculas, lo que determina finalmente la
estabilidad o inestabilidad de las cápsulas a los diferentes pH evaluados.

De acuerdo
a Pérez y col. (2012), el pH en tratamientos de gelificación
iónica debe ser igual o menor a 3.3, para mantener cápsulas estables y de mayor
grado de gelificación. Estos cambios de pH, después
del almacenamiento, se deben quizá por la oxidación que sufre el ácido ascórbico
a ácido dehidroascórbico, así como el incremento de
ácidos orgánicos, que pudieron influir en la reducción de estos valores, lo que
provocó que incrementara el pH al día 12 de
almacenamiento. Las características de los geles de alginato-calcio
pueden ser influenciadas por muchos factores, tales como pH, agente secuestrante, dureza del agua, adición de hidrocoloides y la cantidad de agua, y el pH fue uno de los
factores que más influencia tuvo sobre la estabilidad de las cápsulas en este
estudio, tal como lo observó King (1983), quien determinó que el pH tiene un efecto significativo sobre la formación de
geles de alginato, cuyo rango de pH donde se
obtuvieron los mejores cápsulas es de 2.8 a 4.0.
En la Tabla
3 se muestran las medias de los atributos de color, de las cápsulas obtenidas por
gelificación iónica, al día 0 y al día 12. Los
valores de L* al día 0 en las muestras a 5 ºBrix,
oscilaron de 35.95 a 39.30 a 26 ºC, y de 35.60 a 39.71
a 4 ºC. No se observaron diferencias con respecto a
la concentración de pectina y pH inicial, pero se observó una ligera reducción
al día 12 a 26 ºC (31.93 a 39.41) y a 4 ºC (35.16 a 39.77), lo cual
podría atribuirse a la pérdida parcial de agua, que ocasionó ese ligero descenso. En las cápsulas a 15 ºBrix, la luminosidad inicial fue más homogénea en todos los tratamientos evaluados al día 0 a 26 ºC (35.87 a 38.14) y a 4 ºC (37.59
a 39.45). Este incremento se debe tal vez a la mayor concentración de sólidos
presentes en el jugo, ya que aún al día 12 ocurrió una menor pérdida de pigmentos,
debido a que a baja temperatura la degradación es menor.
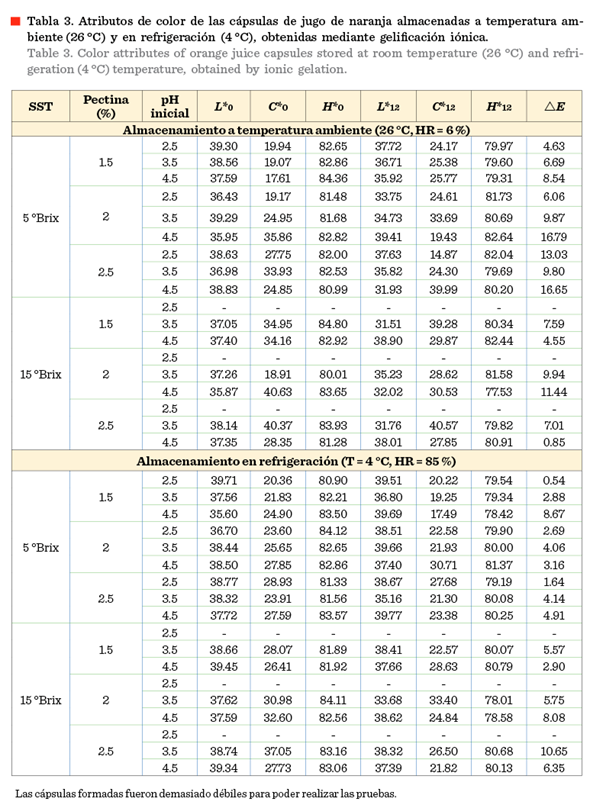
La
saturación de color o cromaticidad (C*) se mantuvo en un rango de 17.61
a 35.86 al día
0 con 5 ºBrix a 26 ºC, y de 20.36 a 28.93
a 4 ºC. No se observó una tendencia clara en este
atributo de color después de 12 d de almacenamiento. A 15 ºBrix,
los valores de C*, de las cápsulas almacenadas a 26 ºC,
fueron similares (18.91 a 40.63) porque el
mayor contenido de sólidos presentes en el jugo se debió a un incremento en los azúcares disueltos.
Con respecto a las cápsulas almacenadas a 4 ºC, los
valores de cromaticidad al día 0 oscilaron
entre 26.41 a 37.05. A los 12 d de almacenamiento se observó una
reducción general de este atributo (21.82 a 33.40), alcanzando valores hasta 17.49 al día 12, a 5 ºBrix
con pectina al 1.5 % (p/v) y pH 4.5. Los materiales de pared de las microcápsulas protegen los componentes encapsulados contra efectos ambientales (oxígeno, luz, humedad, entre otros) lo que mejora su estabilidad, (Garg y col., 2006), lo cual se pudo apreciar en el presente
estudio, ya que la pectina y el alginato
contribuyeron a la estabilidad, de los
pigmentos responsables del atributo de
color.
Los valores
de tonalidad (H*) de las cápsulas almacenadas a 26 ºC
fueron de 80.99 a 84.36 y de 80.01 a 84.80 a
5 ºBrix y 15 ºBrix, respectivamente.
Estos valores se redujeron ligeramente al día 12. Este mismo comportamiento fue observado también en todas
las cápsulas almacenadas en refrigeración,
en todos los tratamientos. Al
parecer, el pH y la concentración de pectina
no tuvieron influencia sobre este parámetro, observándose como
resultado
cápsulas de color amarillo de tonalidad uniforme. En el estudio realizado por Pérez
y col. (2012), indicaron que la modificación en la estabilidad de color, en
esferas realizadas con bebida comercial a
base dejugo de cítricos (naranja, mandarina y limón),
no es
significativa, ya que los valores de L*y H* van en aumento con el
transcurso de los días, lo que da como resultado una estabilidad visual. Estos
resultados muestran similitud con los tratamientos aquí descritos, ya que se
pudo apreciar que la temperatura de
almacenamiento y la humedad relativa en sinergia tuvieron influencia en
los cambios de color y la concentración de los agentes gelificantes utilizados.
El almacenamiento
influyó en la estabilidad de las cápsulas, ya que a pesar de que los materiales
de pared (pectina y alginato de sodio) forman geles
estables al calor, un tratamiento térmico prolongado, a bajo o alto pH desestabiliza
los geles, debido a una tasa de reacción incrementada de procesos de depolimerización, tales como la hidrólisis catalizadas por
protón y las reacciones de b-eliminación, como lo reportó Smidsrod
y Draget (1997), observándose los valores más altos
de DE
a pH 4.5 a 5 ºBrix almacenadas a 26 ºC, y los valores más bajos a bajas temperaturas, lo que ocurrió
quizá debido a la capacidad de las pectinas de formar geles, la cual está
influenciada por el grado de metoxilación y el patrón
de los grupos carboxilo libres que determinan las propiedades funcionales, en
adición a factores ambientales tales como los
iones presentes (calcio principalmente), pH (grado de disociación de los
grupos carboxilo y las concentraciones de
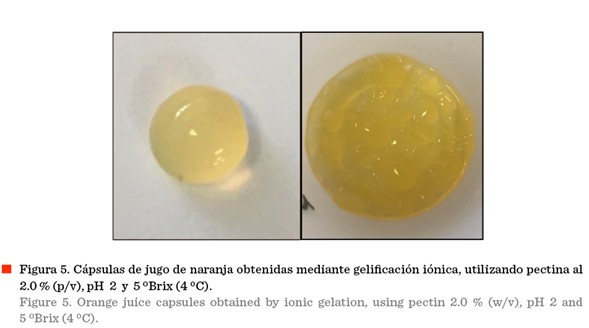
azúcares (Kastner y col., 2019). De acuerdo a lo
anterior, utilizando el método de gelificación iónica
se obtuvieron cápsulas estables (Figura 5). Las que mostraron una mayor estabilidad
durante los 12 d de evaluación fueron las obtenidas a una concentración de pectina
del 2 % (p/v), pH 2.5 y a 5 ºBrix, almacenadas a 4 ºC, lo
cual pudo ser debido a los factores
mencionados anteriormente.
Cabe
mencionar que las formas macroscópicas observadas más frecuente fueron las siguientes: esféricas, ovoides, irregulares y amorfas.
La concentración de pectina, pH y condición de almacenamiento no
tuvieron gran influencia en los cambios físicos de las cápsulas, siendo la
morfología más común la esférica. La concentración inicial de SST fue la variable que más influyó en que se
presentaran morfologías diferentes a las esféricas.
Los tratamientos que obtuvieron los mejores resultados morfológicos
fueron los de menor concentración de SST (5 ºBrix), puesto que obtuvieron un 45.56 % de forma esférica y solo un 6.67 % para cápsulas amorfas;
a pesar de ello, es necesario estandarizar las condiciones aplicadas en la gelificación iónica para incrementar la predominancia de la
morfología esférica, y por tanto, tener un mayor control sobre las propiedades
de las cápsulas. Por otra parte, las cápsulas
con mayor concentración de SST (15 ºBrix) presentaron formas irregulares y amorfas en
la mayoría de sus tratamientos, observándose además durante los 12 d, cierta
degradación de las cápsulas y esta sinéresis fue más frecuente en las cápsulas
amorfas. Las cápsulas elaboradas a partir de alginato
tienden a presentar paredes más rígidas y de mayor porosidad, tal como lo
explican Burey y col. (2008), ya que los alginatos forman un complejo insoluble con el calcio, lo que da pie
a la formación de una pared semirrígida constituida
por enlaces químicos. En esta pared los iones calcio se sitúan como
puentes entre los grupo carboxilo del alginato, dando
lugar a cápsulas de geles estables al tiempo y resistentes a la temperatura.
Las
cápsulas que registraron una menor pérdida de peso, almacenadas a 4 ºC, debieron presentar una pared mejor estructurada, probablemente
más gruesa y estable a los 12 d de evaluación, independiente de sus concentraciones de SST, pectina, pH y condiciónde almacenamiento. Dias y col. (2015) mencionaron que en una técnica de encapsulación,
los materiales, proceso de producción, morfología final y aplicación son los
factores más importantes para ser considerados en sistemas de liberación de
compuestos bioactivos, para que estos puedan ejercer
las funciones biológicas, por lo que mejoran su estabilidad, aplicando técnicas
como la gelificación iónica es una alternativa viable.
CONCLUSIONES
El uso de
tecnologías de encapsulación es adecuado para obtener productos más estables y que
permitan conservar las propiedades fisicoquímicas de los zumos, ya que
utilizando el método de gelificación iónica se
pudieron obtener encapsulados de jugo de
naranja con 5 ºBrix, con parámetros de calidad
aceptables, utilizando alginato de sodio 0.5 % (p/v) y pectina 2 % (p/v) como agentes
encapsulantes, pH 2.5 y almacenados a 4 ºC. Por tanto, el uso de tecnologías de encapsulación como gelificación iónica permitieron preservar las características
fisicoquímicas del jugo de naranja producido en Tamaulipas, que es el segundo
estado citrícola más importante a nivel nacional, lo que contribuirá a mejorar
la comercialización de este producto regional, ofreciendo alternativas que ayuden
a la diversificación de su uso y/o agregarse a otros productos alimenticios.
AGRADECIMIENTOS
Se agradece
a la Subsecretaría de Educación Superior y la Dirección General de Educación
Superior Universitaria por la beca otorgada
para la realización del proyecto de investigación
DSA/103.5/16/10526 dentro del programa de Licenciatura en Nutrición de
la Universidad Autónoma de Tamaulipas.
ReferencIAs
Agulhon, P., Robitzer,
M., Habas, J. P., and Quignard, F. (2014). Influence of both cation and alginate nature on the
rheological behavior of transition metal alginate gels. Carbohydrate
Polymers. 112: 525-531.
Burey, P., Bhandari, B. R., Howes, T., and Gidley, M. J.
(2008). Hydrocolloid gel particles: formation, characterization, and application. Critical Reviews in Food Science and Nutrition. 48(5): 361-377.
Dias,
M. I., Ferreira, I. C., and Barreiro, M. F. (2015). Microencapsulation of bioactives for food
applications. Food & Function.
6(4): 1035-1052.
Draget, K. I. and Taylor, C. (2011). Chemical, physical and
biological properties of alginates and
their biomedical implications. Food
Hydrocolloids. 25(2): 251-256.
Einhorn-Stoll, U. (2018). Pectin-water interactions in
foods–From powder to gel. Food hydrocolloids. 78: 109-119.
Einhorn-Stoll, U., Kastner, H.,
Hecht, T., Zimathies, A., and Drusch,
S. (2015). Modification and physico-chemical
properties of citrus pectin–Influence of enzymatic and acidic demethoxylation. Food Hydrocolloids. 51: 338-345.
García,
C. G., González, M. M., Ochoa, L. M. y Medrano, H. R. (2004). Microencapsulación de jugo de cebada verde mediante secado
por aspersión. Ciencia y Tecnología
Alimentaria. 4(4): 262-266.
Garg, M. L., Wood, L. G., Singh, H., and Moughan, P. J. (2006). Means of delivering recomemended levels of
long chain n-3 polyinsaturated fatty acids in human
diets. Journal of Food Science. 71(5): 66-71.
Gouin, S. (2004). Microencapsulation: industrial appraisal
of existing technologies and trends. Trends in Food Science & Technology. 15(7-8): 330-347.
Kastner, H., Einhorn-Stoll, U., and
Drusch, S. (2019). Influence of enzymatic and acidic demethoxylation on structure formation in sugar containing
citrus pectin gels. Food Hydrocolloids. 89: 207-215.
King, A. H. (1983). Brown seaweed extracts (alginates).
In Martin Glicksman (Ed.), Food Hydrocoloids (pp. 115-183). Florida: CRC Press.
Krasaekoopt, W., Bhandari, B., and Deeth,
H. (2003). Evaluation of encapsulation techniques of probiotic for yoghurt. International
Dairy Journal. 13(1):
3-13.
Licona,
J. C. (2009). Estudio de mercado para identificación de
necesidades de infraestructura logítica para la comercialización
de jugo de cítricos en Veracruz. Martínez de la Torre,
Veracruz: FIRCO. [En línea]. Disponible en: http://www.sagarpa.mx/agronegocios/Documents/Estudios_promercado/SISTPROD_CITRICOS.pd.
Fecha de consulta: 10 de diciembre de 2018.
Li-Ying, N., Ji-Hong, W., Xiano-Jun,
L., Fang, C., Zheng-Fu, W., Guang-Hua, Z., and
Xiao-Song, H. (2008). Physicochemical characteristics of orange juice samples from seven cultivars. Agricultural Sciences in China. 7(1): 41-47.
Liu, Y., Dong, M., Yang, Z., and Pan, S. (2016). Antidiabetic
effect of citrus pectin in diabetic rats and potential mechanism via PI3K/Akt signaling pathway. International Journal of
Biological Macromolecules. 89:
484-488.
Lupo, B. P., González, C.
A., and Maestro, A. G. (2012). Microencapsulación
con alginato en alimentos. Técnicas y aplicaciones. Revista
Venezolana de Ciencia y Tecnología de Alimentos. 3(1): 130-151.
Mohnen, D. (2008). Pectin structure and biosynthesis. Current Opinion
Plant Biology. 11(3): 266-277.
Naqash, F., Masoodi, F. A.,
Rather, S. A., Wani, S. M., and Gani,
A. (2017). Emerging concepts in the nutraceutical and functional properties of
pectin—A Review. Carbohydrate Polymers. 168: 227-239.
Nedovic, V., Kalusevic, A., Manojlovic, V., Levic, S., and Bugarski, B. (2011). An overview of encapsulation
technologies for food applications. Procedia Food Science. 1: 1806-1815.
Orive,
G., Santos, E., Poncelet, D., Hernández, R. M., Pedraz, J. L., Wahlberg, L. U., …, and Emerich, D. (2015). Cell encapsulation: technical and clinical advances. Trends in Pharmacological Sciences.
36(8): 537-546.
Parra,
R. H. (2010). Revisión: Microencapsulación de
Alimentos. Revista Facultad Nacional de
Agronomía Medellín. 63:
5669-5684.
Peanparkdee, M., Iwamoto, S., and Yamauchi, R. (2016).
Microencapsulation: a review
of applications in the food and pharmaceutical
industries. Reviews in Agricultural
Science. 4: 56-65.
Pérez,
L. C., Reyes, K. B., Godines, A. H. y Castillo, R. P.
(2012). Desarrollo y caracterización de golosinas con
ingredientes de intéres nutrimental.
CienciaUAT. 6(3): 50-55.
Rivera,
E. A. T. (2013). Evaluación de la capacidad de esterificación de quitosano como sustituto de alginato
en la elaboración de falso caviar. Tesis de Ingeniería Química de
Alimentos, Universidad Central de Ecuador, Ecuador, Quito. [En línea]. Disponible
en: http://www.dspace.uce.edu.ec/handle/25000/1863. Fecha de consulta: 14 de
enero de 2019.
SAGARPA,
Secretaría de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación
(2015). Situacion de la citricultura en Nuevo León.
Corporación para el desarrollo agropecuario de Nuevo León. [En línea]. Disponible
en: http://www.camponl.gob.mx/oeidrus/docs/citricultura.pdf. Fecha de consulta:
27 de noviembre de 2018.
Sandoval,
M. P., Cu, T. C., Peraza, G. M., and Acereto, P. O.
M. E. (2016). Introducción en los procesos de encapsulación de moléculas nutracéuticas. En M. E. Ramírez-Ortiz (Ed.), Alimentos
Funcionales de Hoy (pp. 181-218). Barcelona, España: Omnia
Science.
Smidsrod, O. and Draget,
K. I. (1997). Alginate gelatión
technologies. In E. Dickenson,
B. Bergenstahl (Ed.), Food
colloids, proteins, lipids and polysaccharides (pp. 279-293).
Lancaster: Ediciones Royal Society of Chemistry.
Venkatesan, J., Lowe, B., Anil, S., Manivasagan, P., Kheraif, A. A.
A., Kang, K. H., and Kim, S. K. (2015). Seaweed polysaccharides and their potential biomedical applications. Starch-Stärke. 67(5-6): 381-390.
Voo, W. P., Ravindra,
P., Tey, B. T., and Chan, E. S. (2011). Comparison of alginate and pectin based beads for
production of poultry probiotic cells. Journal of Bioscience and Bioengineering.
111(3): 294-299.
Willats, W. G. T., Knox, J. P.,
and Mikkelsen, J. D. (2006). Pectin:
New insights into an old polymer
are starting to gel. Trends Food Science Technology. 17(3):
97-104.