La comunidad de peces
del arrecife Palo Seco, Veracruz, golfo de México y su relación con los grupos morfofuncionales
The fish
community of Palo Seco Reef,
Veracruz, gulf of Mexico
and its relationship with the morpho
functional groups
Carlos González-Gándara
*Correspondencia:
cggandara@hotmail.com/Fecha de recepción: 22 de agosto de 2019/Fecha de aceptación: 17 de enero de 2020/Fecha de publicación: 31 de enero de 2020.
Universidad Veracruzana, Facultad de Ciencias Biológicas y Agropecuarias, Laboratorio de Arrecifes Coralinos, carretera Tuxpan-Tampico km 7.5
col. Universitaria, Tuxpan,
Veracruz, México, C. P. 92860.
Resumen
Los bancos arrecifales sumergidos funcionan como áreas de reserva de
germoplasma, debido a su riqueza y abundancia de especies, lo que favorece el desarrollo
de biomasa en arrecifes emergentes vecinos.
El objetivo de la presente investigación fue establecer la comunidad de
peces del arrecife Palo SecoVeracrz, México, y su relación
con los grupos morfofuncionales que caracterizan al sustrato.
Se efectuaron 117 censos visuales con equipo de buceo SCUBA (63 censos
aleatorios y 54 transectos en banda) durante los
veranos de 2013 y 2016, para determinar la estructura de la comunidad de peces
(composición, riqueza, abundancia, biomasa y gremios tróficos) y caracterizar
el sustrato, usando los grupos morfofuncionales (GMF)
a partir de fototransectos. Las relaciones entre los
peces y el sustrato se determinaron mediante
un análisis de correspondencia
canónica (ACC). La ictiofauna de Palo Seco
estuvo compuesta por 109 especies, incluyendo 2 invasoras (Pterois volitans y Neopomacentrus cyanomos), y 3 endémicas de Veracruz (Elacatinus jarocho, Hypoplectrus atlahua
e Hypoplectrus castroaguirrei). Halichoeres burekae, Coryphopterus hyalinus y los juveniles de Haemulon aurolineatum fueron las especies más abundantes,
mientras que, Sphyraena barracuda, Anisotremus virginicus y Megalops atlanticus dominaron en biomasa. El gremio de los zooplanctívoros fue el más abundante (83.35 %)
contrastando con la proporción de herbívoros (1.24 %). Los piscívoros
presentaron la mayor biomasa (28.89 %), seguidos de los carnívoros generalistas
(28.22 %). El sustrato del arrecife se caracterizó por nueve grupos morfofuncionales. En el ACC se observó un gradiente de los
GMF y de la profundidad que se relacionaron con algunas especies de peces y con
algunos gremios tróficos. La comunidad ictiológica del arrecife Palo Seco en
general, se parece a las comunidades de peces de otros arrecifes veracruzanos,
pero su riqueza y abundancia responde a las condiciones locales. El parecido
sugiere una posible conectividad regional y resalta su importancia para la conservación.
Palabras clave:
bancos sumergidos, ictiofauna, suroeste del golfo de
México.
Abstract
The submerged reef banks may play
the part of germoplasm reserve, due to their richness and species abundance that contribute to the biomass development in adjacent emergent reefs. The goal
of this research was to establish the fish community
of Palo Seco Reef, Veracruz, Mexico,
and its relationship with morpho functional groups of the substrate. One hundred and seventeen visual censuses (63 random and 54 belt-transects) using SCUBA dive equipment were carried out during
the Summers of 2013 and
2016 in order to determine the
fish community structure (components, richness, abundance, biomass and trophic guilds) and characterize the substrate based on the
morpho functional groups (MFG). The relationships between the fish and the substrate
were determined by a canonical correspondence analysis (CCA). The ichthyofaune was represented by109 species, including 2 invasive species (Pterois volitans and Neopomacentrus cyanomos), and 3 endemic
species of Veracruz (Elacatinus jarocho,
Hypoplectrus atlahua and Hypoplectrus castroaguirrei). Halichoeres burekae, Coryphopterus hyalinus and juvenile
of Haemulon aurolineatum were
the most abundant species, whereas Sphyraena barracuda,
Anisotremus virginicus and Megalops atlanticus dominated
in biomass. The zooplanctivore guild was the most abundant
(83.35 %), in contrast with
the herbivorous (1.24 %). The piscivorous fish were the
most abundant in biomass (28.89 %), followed by the generalized
carnivorous fish (28.22 %).
Nine MFG characterized the substrate of Palo Seco Reef. The CCA showed a gradient of MFG and depth which were related
to some fish species and to some trophic guilds. The ichthyological community of Palo Seco Reef is similar to the fish communities of other reefs in Veracruz, but its richness and abundance respond to the local environment. The similarity suggests a possible regional connectivity
and underlines its importance for conservation.
Keywords: submerged banks,
ichthyofaune, southwest gulf of Mexico.
Introducción
Los bancos
sumergidos se desarrollan desde el fondo del mar, pero no alcanzan a llegar a
la superficie, probablemente porque no mantuvieron su ritmo de crecimiento para
compensar la tasa de ascenso del nivel del mar durante la trasgresión holocénica o bien porque no llegaron a ese nivel, cuando la
tasa de ascenso se redujo (Neumann y Macintyre, 1985; Abbey y Webster, 2011). Recientemente se ha reconocido su importancia ecológica porque
son un hábitat disponible para los organismos marinos y pueden contribuir de manera significativa a la producción de larvas
(Thomas y col., 2015). Además conectan las
comunidades arrecifales y sirven como áreas de reserva de germoplasma (Ortiz-Lozano y col.,
2013; Thomas y col., 2015; Salas-Monreal y col., 2018).
En las costas
de Veracruz se tienen documentados más de 30 bancos sumergidos (Gobierno del
Estado de Veracruz, 2008; Ortiz-Lozano y
col., 2013; Cortés-Useche y col., 2015; González-Gándara, 2015;
Ortiz-Lozano y col., 2018). Uno de ellos es el arrecife Palo Seco, ubicado en
el sur del estado, muy cerca de la desembocadura del río Coatzacoalcos, lo cual
le confiere una alta turbidez debido a las descargas fluviales (Salas-Pérez y
col., 2015), que reducen la calidad del agua tanto para la comunidad de corales
escleractinios (Loya, 1976) como para la de peces (Wenger y col., 2015a). Esto es, porque los corales se
desarrollan mejor en aguas transparentes, oligotróficas (Zlatarsky
y Martínez-Estalella, 2018), y se vinculan
estrechamente
con la comunidad de peces (Ricart y
col., 2016).
La estructura
de las comunidades de peces se ha relacionado con la profundidad (Hernández-Landa
y col., 2014), la cobertura coralina (Jones y Sims,
1998), la complejidad del ambiente (Aguilar-Medrano y Arias-González, 2018) y la turbidez (Wenger
y col., 2015a; 2015b), entre otros. Los ensambles de peces asociados a los arrecifes de coral veracruzanos,
en general, se conocen bien, tanto en el
Sistema Arrecifal Veracruzano (SAV) (Del-Moral-Flores
y col., 2013 y Robertson y col., 2019) como en el Sistema Arrecifal
Lobos-Tuxpan (SALT) (González-Gándara y
col., 2012; 2013). Sin embargo, se sabe muy poco de la ictiofauna ligada a los bancos sumergidos deVeracruz, ya que únicamente existen 3 trabajos publicados, que aportan información sobre los componentes ictiológicos de los arrecifes:
Blake, Pantepec y Oro Verde, ubicados en el norte del
estado (Cortés-Useche y col., 2015; González-Gándara, 2015), y el registro de Neopomacentrus cyanomos procedente del Indo Pacífico, en Palo
Seco, Veracruz (González-Gándara y De-la-Cruz-Francisco, 2014).
El
conocimiento de la estructura de las comunidades
de peces ligadas a los arrecifes veracruzanos, es necesario para
documentar la conectividad ecológica
planteada por Ortiz-Lozano y col. (2013), que es soportada parcialmente
por los patrones de corrientes del suroeste del golfo de México (Salas-Monreal
y col., 2018). Por otra parte, la Comisión Nacional de Áreas Naturales
Protegidas (CONANP) propuso el Área de
Protección de Flora y Fauna Arrecifes de los Tuxtlas,
en el sur de Veracruz (CONANP, 2018), pero no
incluyó al arrecife Palo Seco.
El objetivo
del presente trabajo fue determinar la estructura de la comunidad de peces en
el arrecife Palo Seco, Veracruz, y su relación
con los grupos morfofuncionales que caracterizan
el sustrato, para enfatizar su importancia ecológica y documentar su incorporación a la propuesta de áreas naturales protegidas.
MATERIALES Y MÉTODOS
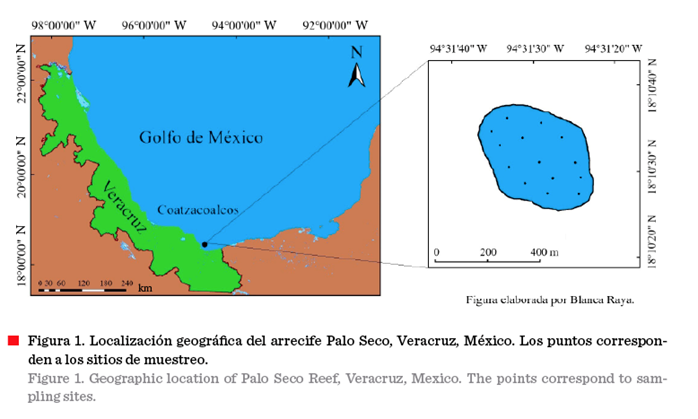
Palo Seco se ubica a los 18°10’30” N y 94°31’30” W, a 1 920 m de la costa de Coatzacoalcos,
Veracruz, y cubre un área aproximada de 0.12 km2 (Figura 1).
Presenta una profundidad que oscila de 11.6 m a 22 m, su estructura arrecifal contiene varios parches con baja cobertura
coralina representada por Pseudodiploria sp, Montastraea sp, Siderastrea sp, Agaricia sp
y Oculina sp. Las
pendientes rocosas contienen numerosas colonias de esponjas e hidroides (González-Gándara y col., 2015). Esta formación
es bañada por el río Coatzacoalcos cuyo gasto en época de lluvias es de 661.44
m3/s, y su temperatura promedio es
de 25.39 °C (Salas-Pérez y col.,
2015).
Se llevaron
a cabo 117 censos visuales en total, 63 usando la técnica de buzo errante con
una duración de 30 min efectuados en junio y
agosto de 2013, para las evaluaciones cualitativas, y 54 transectos
en banda (25 m x 2 m), distribuidos sistemáticamente en 14 sitios en el arrecife (Figura 1), para
los muestreos cuantitativos
efectuados en junio de 2016. Los puntos de muestreo se seleccionaron de forma
tal, que estuviesen distribuidos en toda el área del arrecife y permitieran un muestreo
entre 11.6 m y 22.0 m de profundidad. Ambos muestreos se hicieron con equipo de
buceo autónomo SCUBA. La identificación de los peces fue realizada in situ
a partir de los rasgos morfológicos y los patrones de coloración que distinguen
a los peces arrecifales.
Cuando esto no fue posible, se llevaron a cabo recolectas; los peces mayores a
10 cm de longitud total se capturaron con
hawaianas, y los peces menores a 10 cm de longitud total fueron rociados
con una solución de aceite de clavo (10 % aceite de clavo y 70 % etanol) para adormecerlos, y luego se atraparon
con redes de mano. Los organismos se
transportaron al laboratorio para su identificación, utilizando las
obras de Böhlke y Chaplin (1993) y McEachran y Fechhelm (1998;
2005). La nomenclatura fue revisada usando el catálogo de peces (Fricke y col., 2018). La lista fue ordenada de acuerdo con
Nelson y col. (2016), para las categorías supragenéricas; los géneros y especies se ordenaron
alfabéticamente. La suficiencia del muestreo fue determinada utilizando los estimadores
no paramétricos: Chao 2, Jack 1, Jack 2 y Bootstrap, con el programa EstimateS
versión 9.0 (Colwell, 2013), considerando el número
total de censos (117).
La
estimación de la abundancia ictiológica se realizó sobre los 54 transectos en banda (25 m x 2 m), utilizando la escala propuesta
por Harmelin-Vivien y col. (1985): 1, 2, 3 a 5; 6 a
10; 11 a 30, 31 a 50, 51 a 100, 101a 200, 201
a 500 y > 500. Las tallas fueron estimadas considerando intervalos de
10 cm (1 cm a 10 cm; 11 cm a 20 cm; 21
cm a 30 cm, 31 cm a 40 cm, 41 cm a 50 cm; 51
cm a 60 cm, 61 cm a 70 cm, 71 cm a 80 cm, entre otros), posteriormente,
se calculó la talla media. Para validar las estimaciones de talla efectuadas
por el buzo, se realizó una prueba t- pareada,
siguiendo la propuesta de English y col. (1997), usando el programa PAST
versión 3.25 (Hammer y col., 2001). A partir de los datos
de abundancia y de talla promedio de cada especie, se evaluó la biomasa mediante
la función exponencial P = a Lb, donde, P = peso total (g) L =
longitud total (cm); a y b = constantes de la relación peso-longitud. Los
valores de estas constantes se obtuvieron a partir de la base de datos
electrónica Fishbase (Froese y Pauly, 2019) y la publicación de: Claro y García-Arteaga
(1994). Las especies de peces, registradas durante la evaluación cuantitativa
se agruparon con base en su nivel trófico, siguiendo la propuesta de Randall (1967), que considera los siguientes
grupos: carnívoros generalistas, consumidores de
invertebrados con concha, consumidores de invertebrados sésiles, ectoparasitívoros,
herbívoros, omnívoros, piscívoros y zooplanctívoros,
para valorar su aporte a la abundancia
total.
Los componentes
bentónicos fueron determinados usando los siguientes grupos morfofuncionales:
algas césped, algas costrosas, cianobacterias, corales, esponjas, macroalgas, arena, materia orgánica y roca, definidos a partir
de 1 470 fotografías tomadas sobre los transectos de
25 m x 2 m con una cámara Canon, Power Shot
G16 de 16 megapíxeles (Tokio, Japón). Las imágenes fueron analizadas con
el programa Coral Point Count (Kohler
y Gill, 2006), usando 25 puntos al azar por imagen. Para el análisis de
correspondencia canónica (ACC), se utilizó la matriz de cobertura de los grupos morfofuncionales y
la profundidad, previa transformación a Box Cox, contra la matriz de las
especies de peces más abundantes
(transformadas a raíz cuarta) y la matriz
de los gremios tróficos de peces, utilizando el programa PAST versión 3.25 (Hammer
y col., 2001).
RESULTADOS
La fauna
ictiológica del arrecife Palo Seco estuvo constituida por 109 especies pertenecientes
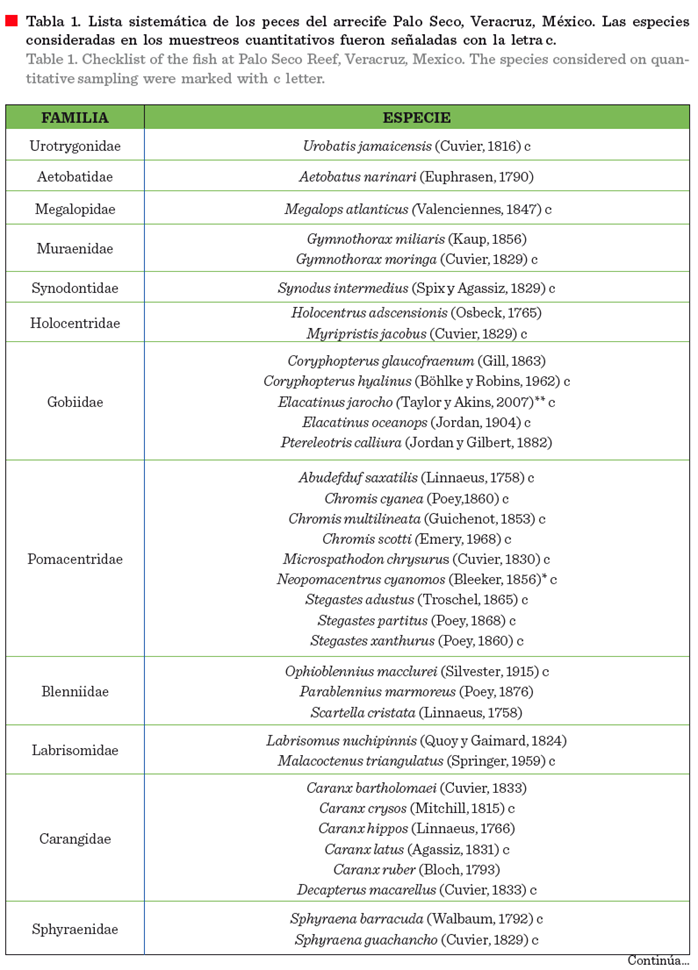
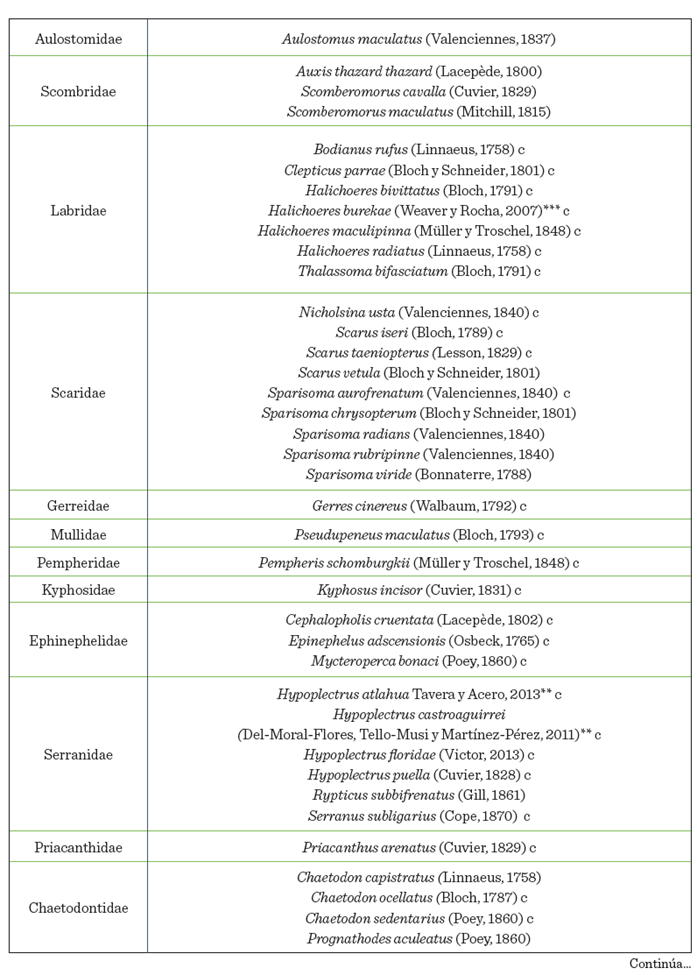
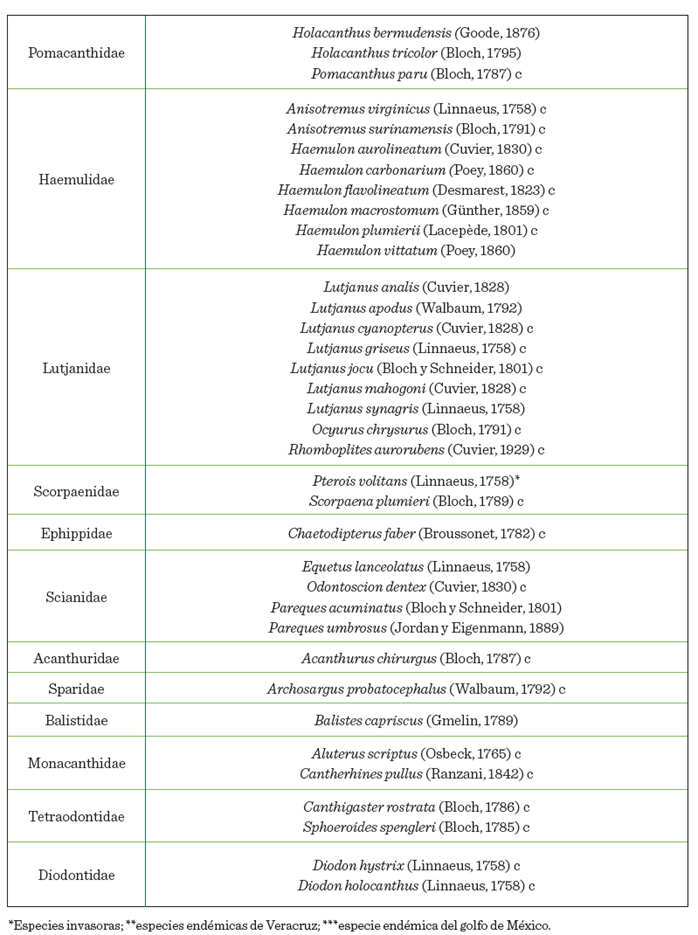
a 67 géneros y 36 familias. Pomacentridae, Scaridae y Lutjanidae fueron las
familias con mayor riqueza, con 9 especies cada una (Tabla 1). Además, se
registró la presencia de 2 especies invasoras: Pterois volitans y N. cyanomos, así como 3 especies endémicas de
Veracruz (Elacatinus jarocho,
Hypoplectrus atlahua e Hypoplectrus castroaguirrei) y 1 del golfo de México (Halichoeres burekae). Los estimadores no paramétricos explicaron
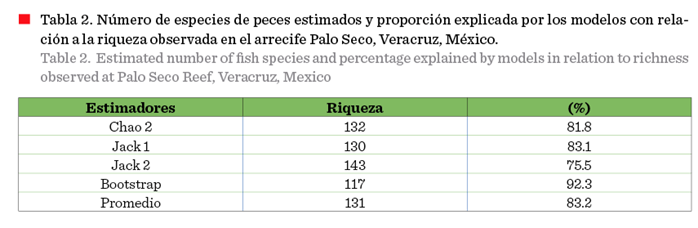
en promedio, el 83.2 % de la riqueza, y potencialmente se pueden registrar
hasta 131 especie (Tabla 2).
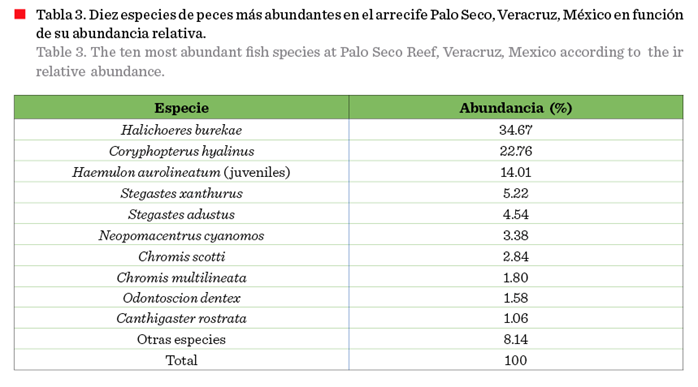
Se contabilizaron
un total de 26 192 individuos, por lo que, la abundancia promedio de peces por
censo fue de 485 ± 148 ind, y entre las especies más
abundantes destacan aquellas de talla menor a 10 cm, como: H. burekae, Coryphopterus
hyalinus y los juveniles de Haemulon aurolineatum que representaron más del 70 % del total
(Tabla 3). La prueba t para la estimación de tallas, no mostró diferencias
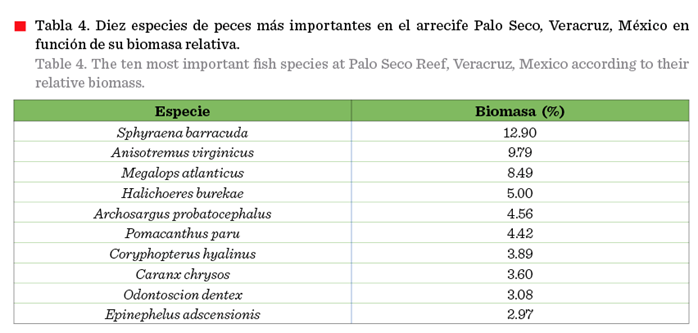
significativas (t = 0.21, P = 0.832). Se estimó una biomasa total de 10 194.05
g durante la investigación, por tanto, el promedio de la biomasa ictiológica
fue de 188.77 ± 169.22 g/m2 por censo. Las especies con mayor
biomasa fueron: Sphyraena barracuda, Anisotremus virginicus
y Megalops atlanticus, representando un poco más del 30 %
(Tabla 4).
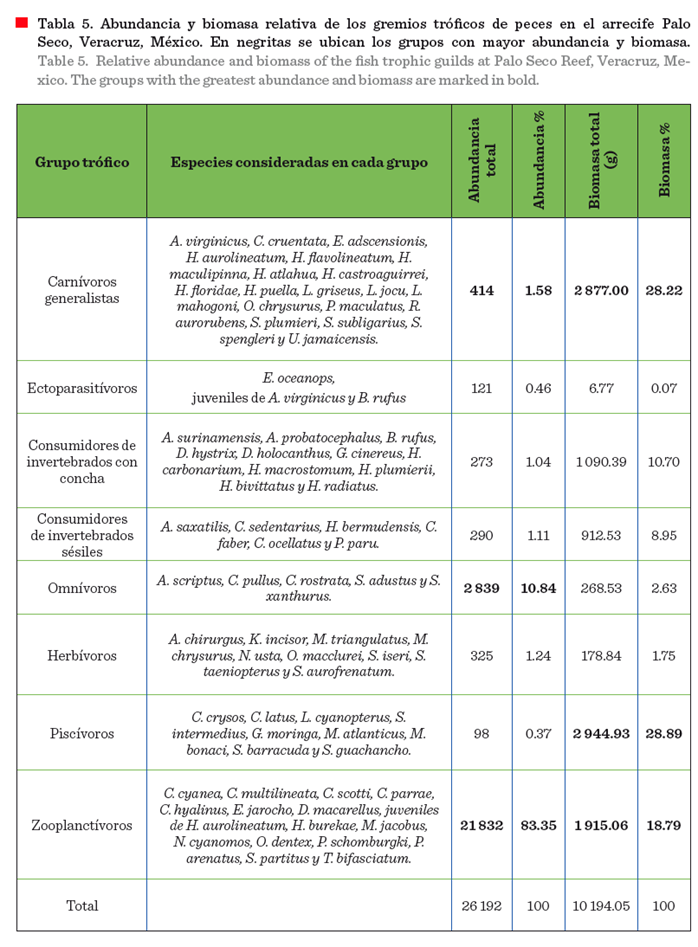
Los peces que
se alimentan de zooplancton (e. g. H.
burekae, C. hyalinus y juveniles de H. aurolineatum) constituyeron el gremio dominante en el
arrecife Palo Seco, representando el 83.35 % del total de la abundancia, seguido de los omnívoros (10.84 %) y carnívoros
generalistas (1.58 %). Al considerar la biomasa,
los zooplanctívoros aportaron el 18.79 %, y
los piscívoros (e. g. M. atlanticus) junto
con los carnívoros generalistas (e. g. Lutjanus jocu) aportaron el 57.11 % al total, debido a que sus tallas, en general, fueron
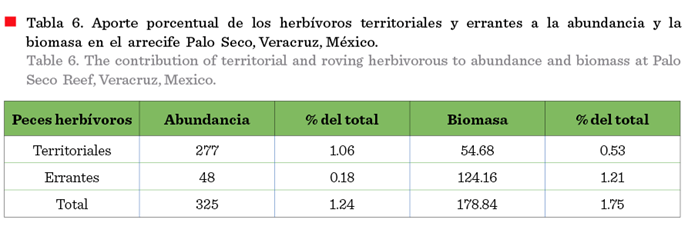
mayores a 20 cm. La proporción de herbívoros en el arrecife Palo Seco fue notablemente reducida tanto en abundancia
total (1.24 %) como en biomasa total (1.75 %) (Tabla 5), especialmente por la
escasa abundancia de herbívoros errantes (escáridos, acantúridos y kifósidos), que
representaron el 0.18 % de la
abundancia total de herbívoros y el
1.21 % de la biomasa total de este gremio (Tabla 6).
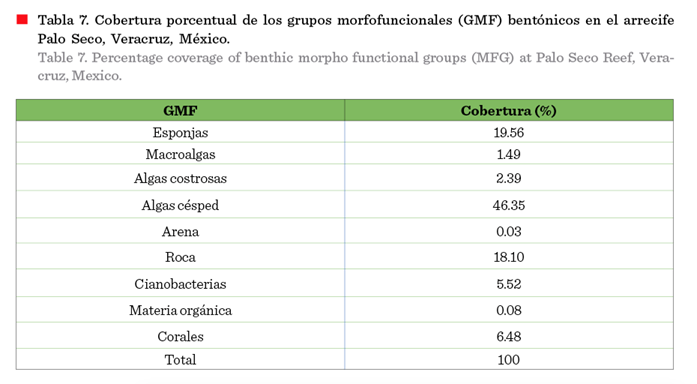
Entre los
GMF que caracterizan al sustrato del arrecife Palo Seco destacaron: algas césped,
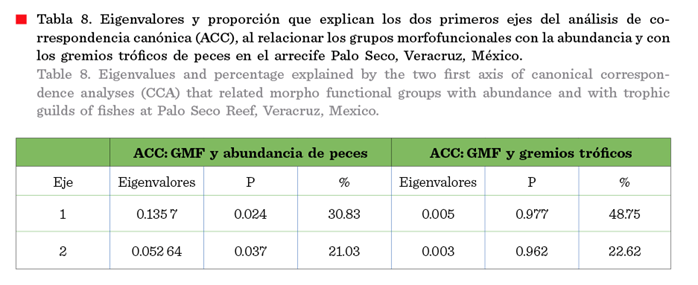
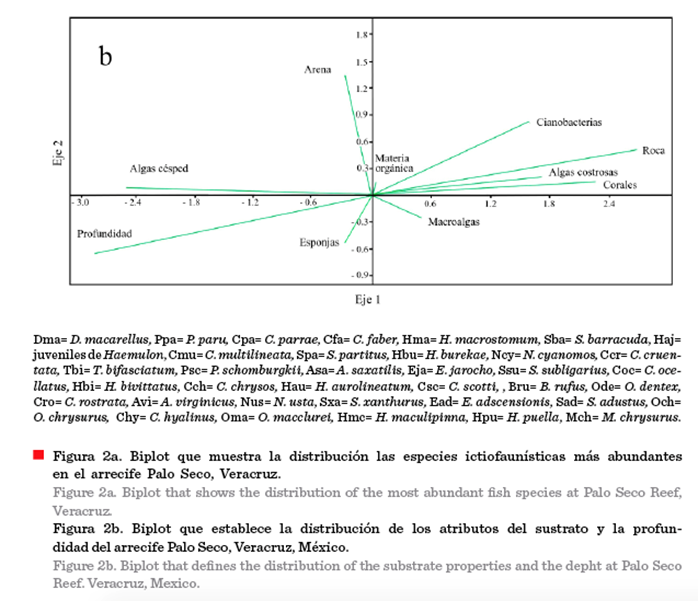
esponjas, roca, corales y cianobacterias (Tabla 7). En el análisis de ACC, el
eje 1 mostró una relación con la proporción de esponjas y de arena. En cambio,
en el eje 2 se detectó un gradiente de la profundidad y las algas césped, que
se relacionan negativamente con la cobertura coralina, de algas costrosas y roca
(Figura 2b). Los eigenvalores fueron relativamente
bajos (Tabla 8), pero se puede detectar una tendencia en la distribución de las
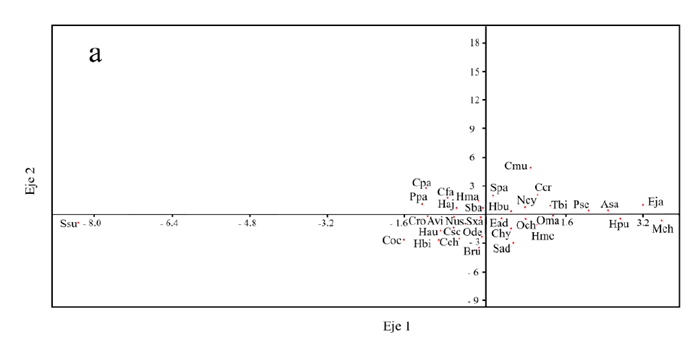
especies de peces en función de la profundidad y la cobertura coralina principalmente.
De esta forma, en las áreas someras con mayor cobertura coralina, fueron más
frecuentes: Microspathodon chrysurus, Abudefduf saxatilis, Elacatinus jarocho, Hypoplectrus puella
y Ophioblennius macclurei, entre otros, mientras que en las zonas profundas
con mayor cobertura de algas césped, fueron
comunes: Serranus subligarius, Chaetodon ocellatus y Pomacanthus paru (Figura 2a, 2b). Los primeros dos ejes del ACC del
GMF y abundancia de peces
explicaron el
51.86 % de
la variación (Tabla 8).
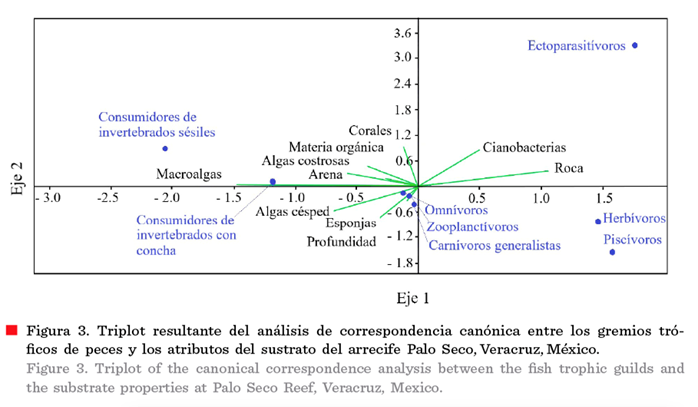
La relación
de los GMF con los gremios tróficos de peces de acuerdo al ACC, no muestra
tendencias claras, sin embargo, se observó que los herbívoros se ligan a la presencia
de roca y cianobacterias, y los consumidores de invertebrados (con concha y
sésiles), se asociaron a las áreas de arena y de mayor cobertura de macroalgas, algas costrosas y algas césped, las cuales
visitan para buscar alimento (Figura 3). Los primeros dos ejes del
ACC del GMF y gremios tróficos explicaron el 71.37 % de la variación
(Tabla 8).
DISCUSIÓN
La riqueza
y abundancia ictiológica en formaciones arrecifales
se ha relacionado positivamente con la cobertura coralina (Jones y Sims, 1998; Wilson y col., 2006; Hernández-Landa y col., 2014;
Ricart y col., 2016) y la complejidad de las colonias
de coral (Álvarez-Filip y col., 2011), entre otros.
Sin embargo, en este estudio, los valores de
la cobertura de corales (6.48 %), así como la complejidad en el arrecife
Palo Seco (0.29) fueron bajos, y por tanto no coincide con la generalización señalada.
La riqueza ictiológica observada en Palo Seco es ligeramente menor a la registrada
en otros bancos sumergidos de Veracruz, como el Blake (126 especies) (Cortes-Useche
y col., 2015; González-Gándara, 2015), y mayor a la observada en los arrecifes:
Pantepec y Oro Verde (42 especies) (Cortés-Useche y
col. 2015). Las diferencias con los 2 últimos, probablemente se relacionen con
el esfuerzo de muestreo. Las estimaciones de la riqueza ictiológica potencial
efectuadas con los modelos no paramétricos son adecuadas, dado que explican más
del 80 % (Tabla 2), 24 especies correspondieron a observaciones únicas y 11
fueron avistadas en 2 ocasiones. Entre los componentes ictiológicos del
arrecife Palo Seco destacan, 3 especies endémicas de Veracruz (E. jarocho, H. atlahua e H. castroaguirrei) y una del
golfo de México (H.
burekae), así como N. cyanomos (González-Gándara y De-la-Cruz-Francisco,
2014) y P. volitans,
originarias del Indo Pacífico.
Las especies de peces más abundantes en Palo Seco coinciden con aquellas
registradas por
González-Gándara
y González-Sansón (1997), para
el arrecife Tuxpan, y Pérez-España y col. (2015) para el SAV. Entre las 10
especies más abundantes en Palo Seco,
destaca N.
cyanomos, lo cual sugiere el
establecimiento definitivo
de esta especie en la región, hecho que puede
influir en la estructura comunitaria, aunque esta aseveración requiere de estudios poblacionales detallados. Uno de los grupos de peces más abundantes corresponde a los territoriales
(e. g. Stegastes adustus y Stegastes xanthurus, posiblemente por su capacidad para
controlar los niveles de sedimentación en sus
territorios, ya que al remover las partículas aseguran el crecimiento de las
algas que prefieren (Ceccarelli y col., 2005 y Dromard y col., 2018). La ausencia de Stegastes planifrons en el área estudiada, parece relacionarse
con la escasez de refugios, especialmente
porque esta damisela se le ha asociado a colonias de los géneros Orbicella o Acropora (Tolimieri, 1998;
González-Gándara y Arias-González, 2004, Dromard y col., 2018), los cuales prácticamente no
existen en el sistema Palo Seco.
La talla de
los peces es determinante en el aporte de
las especies a la biomasa en los sistemas arrecifales.
La presencia de peces de gran talla (mayor a 20 cm) en el arrecife Palo Seco particularmente de piscívoros (e. g. S. barracuda
y M. atlanticus)
y carnívoros generalistas (e.
g. A. virginicus), incrementó su contribución
a la biomasa. Uno de los grupos que menos aportó a la biomasa fue el de
los herbívoros, lo cual es atribuido a las condiciones de turbidez que limitan
la visión e influye en sus valores de
abundancia (Cheal y col., 2013).
El arrecife
Palo Seco se caracteriza por una notable turbidez que resulta de su cercanía a la
costa (Ajemian y col., 2015), y particularmente del volumen de descarga del río Coatzacoalcos,
cuyo promedio anual es de 561.9 m3/s (Salas-Pérez y col.,
2015). La turbidez influye en la riqueza y abundancia de peces (Utne-Palm, 2002; Wenger y col.,
2015b), especialmente de los herbívoros
errantes, debido a que, la concentración de sedimentos suspendidos
limita la transparencia del agua (Cheal y col.,
2013). Por eso, la abundancia de acantúridos, escáridos y kifósidos en el
arrecife Palo Seco, fue muy baja (0.18 %) y contrasta con las observaciones de
González-Gándara y González-Sansón (1997) y Pérez-España y col. (2015),
efectuadas en arrecifes del norte y centro de Veracruz, donde la turbidez es menor
y varias especies de herbívoros errantes son abundantes (e. g. Scarus iseri).
Por otra
parte, los ambientes turbios favorecen a los peces planctívoros,
porque la turbidez les permite visualizar mejor a la presa (Utne-Palm,
2002). En general, las especies de peces más abundantes (H. burekae, C. hyalinus y juveniles de H. aurolineatum) en Palo Seco fueron zooplanctívoras,
lo cual se atribuye a la gran concentración de nutrientes procedentes del río
Coatzacoalcos. Por su parte, los carnívoros
generalistas (Haemulidae,
Lutjanidae) que consumen bentos móvil, como: anélidos,
crustáceos y pequeños peces (Randall, 1967) representaron el 1.58 % de la
abundancia total. Esta baja proporción sugiere
una relación con la estructura de las colonias
coralinas, cuya forma aplanada en Palo Seco, reduce la disponibilidad de
refugios que requieren los peces, especialmente los piscívoros residentes y los
carnívoros genera listas.
El ACC no
dejó evidencias claras de la relación de la comunidad de peces y los GMF en el
arrecife Palo Seco, dado que los eigenvalores son
bajos, y los primeros dos ejes explican únicamente el 51.86 % de la variación. Sin
embargo se nota, que algunas especies territoriales, como M. chrysurus y O. macclurei se ligan a las zonas someras, donde la roca,
algas costrosas, corales y cianobacterias fueron más abundantes, y otras (e. g. S. subligarius y C. ocellatus) se asociaron a las zonas profundas, con
menor cobertura coralina y alta proporción de algas césped. La cobertura coralina
(6.48 %) del arrecife Palo Seco, sugiere una limitada penetración de luz, debido
a los sedimentos suspendidos (observación personal)
y a la profundidad (Wenger y col., 2015b) pero
al parecer, no es determinante en la riqueza y abundancia de peces en Palo
Seco.
El ACC
entre GMF y gremios tróficos provee una limitada descripción de la
interrelación, y la mayor parte de las variables ambientales se ligan al eje 1,
que refleja la relación de los herbívoros con
la presencia de roca y cianobacterias,
a pesar de que este grupo trófico fue escaso, posiblemente debido a la disminución
de la penetración de luz, característica de los sistemas con alta turbidez (Cheal y col., 2013; Fabricius y
col., 2014).
Por su
parte, los peces que se alimentan de invertebrados con concha y de
invertebrados sésiles, se ubicaron en las
zonas de arena donde hurgan en el sedimento o bien en las zonas de mayor
proporción de vegetación (macroalgas, algas césped),
donde se localizan anélidos, moluscos y crustáceos, que utilizan como alimento
(Randall, 1967). Los peces piscívoros no muestran relación clara con el ambiente,
porque la mayor parte de ellos son transeúntes de la columna de agua (M. atlanticus y S. barracuda),
y sugiere una mayor adaptación de estos a las condiciones de turbidez para detectar a sus presas (Huber y Rylander, 1992).
CONCLUSIONES
El parecido
general de los ensambles ictiológicos del arrecife Palo Seco con otros sistemas
arrecifales veracruzanos sugiere la existencia de una
conectividad temporal. Las diferencias puntuales resaltan de las condiciones
ambientales locales definidas por la profundidad y los grupos morfofuncionales del sustrato. La riqueza y abundancia de
los ensambles de peces en los bancos sumergidos, representan una oportunidad
para generar áreas de reserva ecológica, por lo que, el arrecife Palo Seco debe ser incluido en la propuesta de Área de Protección
de Flora y Fauna Arrecifes de Los Tuxtlas,
especialmente porque representa una buena parte de la riqueza biológica
característica de los arrecifes veracruzanos e incluye especies endémicas.
AGRADECIMIENTO
Se agradece
el apoyo de la Secretaría de Educación Pública a través del proyecto “Bases para
el Análisis y Síntesis de los Sistemas Costeros de Veracruz”, realizado en el
marco de la Red para el Análisis y Síntesis de la Zona Costera Veracruzana,
golfo de México.Los muestreos del año 2013 formaron
parte del proyecto “Esponjas, corales escleractinios,
equinodermos y peces de los arrecifes coralinos del norte y sur de Veracruz” (Convenio:
FB1628/JF124/12) financiado por la CONABIO. Se agradece el permiso de pesca de
fomento emitido por la SAGARPA (DGOPA.5458.170512.1381). Se agradecen los
comentarios de los revisores que permitieron mejorar el presente manuscrito.
ReferencIAs
Abbey, E. and Webster,
J. M. (2011). Submerged Reefs.
In D. Hopley (Ed.), Encyclopedia
of Modern Coral Reefs: Structure,
Form and Process (pp.
1058-1062). Netherlands: Springer.
Aguilar-Medrano,
R. and Arias-González, J. E. (2018). Functional reef fish groups
of the Mexican Caribbean: implications of habitat complexity. Revista
Mexicana de Biodiversidad. 89(4): 1138-1153.
Ajemian, M. J., Sohel,
S., and Mattila, J. (2015). Effects
of turbidity and habitat complexity on antipredator behavior of three-spined sticklebacks (Gasterosteus
aculeatus). Environmental
Biology of Fishes.
98(1): 45-55.
Álvarez-Filip, L., Gill, J. A., and Dulvy
N. K. (2011). Complex reef architecture supports more smallbodied fishes and longer food chains
on Caribbean reefs. Ecosphere.
2(10): 1-17.
Böhlke, J. E. and Chaplin, C. C. G.
(1993). Fishes
of the Bahamas and adjacent
tropical waters. Texas: University of Texas Press. 771 Pp.
Ceccarelli, D. M., Jones, G.
P., and McCook, L. J. (2005). Effects
of territorial damselfish on
an algal-dominated coastal coral reef. Coral
Reefs. 24(4):606-620.
Cheal, A. J., Emslie,
M., MacNeil, M. A., Miller, I., and Sweatman, H. (2013). Spatial variation in the functional characteristics of herbivorous fish communities and the resilience of coral reefs. Ecological Applications. 23(1):
174-188.
Claro,
R. y García-Arteaga, J. P. (1994). Crecimiento. En R. Claro (Ed.), Ecología
de los peces marinos de Cuba (pp. 321-402). México: CIQRO.
Colwell, R. K. (2013). EstimateS:
Statistical estimation of species richness and shared species from samples (Version
9.0) . [En línea]. Disponible en: http://viceroy.eeb.uconn.edu/estimates/.
Fecha de consulta: 10 de julio de 2018.
CONANP,
Comisión Nacional de Áreas Naturales Protegidas (2018).
Estudio Previo Justificativo para la declaratoria del Área de Protección de
Flora y Fauna Arrecifes de Los Tuxtlas.
México: Comisión Nacional de Áreas Naturales Protegidas, Secretaría de Medio
Ambiente y Recursos Naturales. México. 180 Pp.
Cortés-Useche,
C., Calle-Triviño, J. y Martos-Fernández, F. J. (2015). Lista de peces de los
arrecifes: Oro Verde, Pantepec y Blake Veracruz,
México. Revista
de Investigaciones Marinas. 35(1): 112-118.
Del-Moral-Flores,
L. F., Tello-Musi, J. L., Reyes-Bonilla, H.,
Pérez-España, H., Martínez-Pérez, J. A., Horta-Puga, G., y
Álvarez-del-Castillo-Cárdenas, P. A. (2013). Lista sistemática y afinidades zoogeográficas de la ictiofauna
del Sistema Arrecifal Veracruzano, México. Revista
Mexicana de Biodiversidad. 84(3): 825-846.
Dromard, C. R., Bouchon-Navaro,
Y., Cordonnier, S., Harmelin-Vivien,
M., and Bouchon, C. (2018). Microhabitat
characteristics of Stegastes
planifrons and Stegastes
adustus territories. Environmental Biology of Fishes. 101(3):
441-448.
English,
S., Wilkinson, C., and Baker, V. (1997). Survey
manual for tropical marine resources. Townsville: Australian Institute of Marine Sciences. 390 Pp.
Fabricius, K. E., Logan, M., Weeks, S., and Brodie, J. (2014).
The effects of river run-off on water clarity across
the central Great Barrier Reef. Marine Pollution
Bulletin. 84(1-2): 191-200.
Fricke, R., Eschmeyer,
W. N., and van-der-Laan, R. (2018). Online database on genus
and species names of recent fishes. [En línea].
Disponible en: http://researcharchive.calacademy.org/research/ichthyology/catalog/fishcatmain.asp.
Fecha de consulta: 12 de julio de 2018.
Froese, R. and Pauly,
D. (2019). FishBase (version
Feb 2018). In Y. Roskov, G. Ower,
T. Orrell, D. Nicolson, N. Bailly, P. M. Kirk, …, and L. Penev
(Eds.), Species
2000 & ITIS Catalogue of Life, 2019 Annual Checklist. [En
línea]. Disponible en: http://www.catalogueoflife.org/annual-checklist/2019.Fecha
de consulta: 12 de abril de 2019.
Gobierno
del Estado de Veracruz (2008). Veracruz y su turismo submarino.
Xalapa, Veracruz, México: Gobierno de Veracruz y Secretaría de Turismo. 128 Pp.
González-Gándara,
C. (2015). Peces del arrecife Blake, Veracruz, México: Inventario, distribución
y afinidades zoogeográficas. Ecosistemas
y Recursos Agropecuarios. 2(4): 87-98.
González-Gándara,
C. y Arias-González, J. E. (2004). Los pomacéntridos
del Arrecife Alacranes, Yucatán, México: composición, distribución y abundancia.
Revista
de Investigaciones Marinas. 25: 231-239.
González-Gándara,
C., and De-la-Cruz-Francisco, V. (2014). Unusual
record of the Indo-Pacific pomacentrid Neopomacentrus
cyanomos (Bleeker, 1856) on coral reefs of the Gulf
of Mexico. Bioinvasion
Records. 3(1): 49-52.
González-Gándara,
C., De-la-Cruz-Francisco, V.,Salas-Pérez,
J. J. y Domínguez-Barradas, C. (2012). Lista de los peces de Tuxpan, Veracruz,
México. UDO
Agrícola. 2(3): 675-689.
González-Gándara,
C. y González-Sansón, G. (1997). Composición y abundancia de la ictiofauna del arrecife
Tuxpan, Veracruz, México. Revista de Investigaciones Marinas.
18(3): 249-259.
González-Gándara,
C., Lozano-Vilano, M. L., De-la Cruz-Francisco, V. y Domínguez-Barradas, C.
(2013). Peces del sistema arrecifal Lobos-Tuxpan,
Veracruz, México. Universidad y Ciencia.
29(2): 191-208.
González-Gándara,
C., Solís-Marín, F. A., De-la-Cruz-Francisco, V., Granados-Barba, A.,
Salas-Pérez, J. J., Arguelles-Jiménez, J. y Escárcega-Quiroga, P. A. (2015).
Riqueza y distribución de equinodermos en los arrecifes del norte y sur de
Veracruz, México. Revista de Biología Tropical. 63(2):
183-193.
Hammer, Ø., Harper,
D. A. T., and Ryan, P. D. (2001). PAST: Paleontological statistics software
package for education and data analysis
(Versión 3.25). [En línea]. Disponible en: http//folk.uio.no/ohammer/past/. Fecha de
consulta: 8 de mayo de 2019.
Harmelin-Vivien, M. L., Harmelin, J. G., Chauvet, C., Duval, C., Galzin, R., Lejeune, P., …, and Laserre, G. (1985). Evaluation visuelle des peuplements et populations de poisons: Méthodes et problèmes. Revue
d’ Ecologie (Terre
Vie). 40: 467-539.
Hernández-Landa,
R. C., Acosta-González, G., Nuñez-Lara, E., and
Arias-González, E. A. (2014). Spatial distribution of surgeonfish and parrotfish in the north sector of the Mesoamerican Barrier Reef System. Marine Ecology.
36(3): 432-446.
Huber,
R. and Rylander, M. K. (1992). Quantitative
histological study of the optic-nerve in species of minnows (Cyprinidae, Teleostei) inhabiting clear and turbid water. Brain
Behavior and Evolution. 40(5):
250-255.
Jones,
G. P. and Syms, C. (1998). Disturbance,
habitat structure, and the ecology of fishes on coral reefs. Australian
Journal of Ecology.
23(3): 287-2297.
Kohler, K. E. and Gill, S. M. (2006).
Coral Point Count with
Excel extensions (CPCe): A
Visual Basic program for the determination of coral and substrate coverage using random point
count methodology. Computers
and Geosiences. 32(9):1259-1269.
Loya,
Y. (1976). Effects of water
turbidity and sedimentation on the community
structure of Puerto Rican corals. Bulletin
of Marine Sciences. 26(4): 450-466.
McEachran, J. D. and Fechhelm,
J. D. (1998). Fishes
of the Gulf of Mexico. (Vol 1). Myxiniformes
to Gasterosteiformes. Texas: University of Texas Press. 1112 Pp.
McEachran, J. D. and Fechhelm,
J. D. (2005). Fishes
of the Gulf of Mexico. Vol 2: Scorpaeniformes to Tetraodontiformes.
Texas: University of Texas Press. 1004 Pp.
Nelson,
J. S., Grande, T. C., and Wilson, M. V. H. (2016). Fishes
of the World. New
Jersey: John Wiley & Sons.
707 Pp.
Neumann,
A. C. and Macintyre, I. (1985). Reef
response to sea level rise:
keep-up, catch-up or give-up. Proceedings
of the Fifth International
Coral Reef Congress. 3: 105-110.
Ortiz-Lozano,
L. D., Colmenares-Campos, C., and Gutiérrez-Velázquez, A. (2018). Submerged Coral Reefs in the Veracruz Reef System, Mexico, and its implications for marine protected area management. Ocean
& Coastal Management. 158:
11-23.
Ortiz-Lozano,
L. D., Pérez-España, H., Granados-Barba, A., González-Gándara, C.,
Gutiérrez-Velázquez, A., and Martos, J. (2013). The Reef Corridor of the Southwest Gulf
of Mexico: Challenges for its management and conservation. Ocean
& Coastal Management. 86: 22-32.
Pérez-España,
H., Ávila-Gutiérrez, P. S., Melo-Merino, S. M., Berumen-Solórzano,
P. y Flores-Arévalo, R. R. (2015). Patrones interanuales e interarrecifales
de las comunidades de peces, corales y equinodermos en el Sistema Arrecifal Veracruzano. En A. Granados-Barba, L. D.
Ortiz-Lozano, D. Salas-Monreal y C. González-Gándara (Eds.), Aportes
al conocimiento del Sistema Arrecifal Veracruzano.
Hacia el corredor arrecifal del suroeste del Golfo de
México (pp. 159-178). Campeche: Universidad Autónoma de Campeche.
Randall,
J. E. (1967). Food habits
of reef fishes of the West Indies. Studies
in Tropical Oceanography. 5:
665-847.
Ricart, A. M., Rodríguez-Zaragoza, F. A.,
González-Salas, C., Ortiz, M., Cupul-Magaña, A. L.,
and Adjeroud, M. (2016). Coral reef
fish assemblages at Clipperton Atoll (Eastern
Tropical Pacific) and their
relationship with coral cover. Scientia
Marina. 80(4): 479-486.
Robertson,
D. R., Domínguez-Domínguez, O., Lopez-Aroyo, Y. M.,
Moreno-Mendoza, R., and Simoes, N. (2019). Reef-associated fishes from the offshore reefs of western Campeche Bank, Mexico,
with a discussion of mangroves and seagrass beds as nursery habitats. ZooKeys:
843: 71-115.
Salas-Monreal,
D., Marín-Hernández, M., Salas-Pérez, J. J., Salas-de-León, D. A.,
Monreal-Gómez, M. A., and Pérez-España, H. (2018). Coral reef connectivity within the Western Gulf of Mexico. Journal
of Marine Systems. 179: 88-99.
Salas-Pérez,
J. J., Ocaña-Valencia, A. N. y González-Gándara, C. (2015). Temperatura
superficial del mar y concentración de Clorofila-a en zonas arrecifales
y desembocadura de sus ríos en el golfo de México Occidental. En A.
Granados-Barba, L. D. Ortiz-Lozano, D. Salas-Monreal y C. González-Gándara
(Eds.), Aportes
al conocimiento del Sistema Arrecifal Veracruzano.
Hacia el corredor arrecifal
del suroeste del Golfo de México (pp. 315-332).
Campeche: Universidad Autónoma de Campeche.
Thomas,
C. J., Bridge, T. C., Figueiredo, J., De-leersnijder, E., and Hanert, E.
(2015). Connectivity between
submerged and near-sea-surface coral reefs: can submerged reef populations act as refuges? Diversity
and Distributions. 21(10): 1254-1266.
Tolimieri, N. (1998). Contrasting
effects of microhabitat use
on large-scale adult abundance in two families of Caribbean reef fishes. Marine Ecology Progress Series.
167: 227-239.
Utne-Palm, A. C. (2002). Visual feeding of fish in a turbid environment: Physical and behavioural aspects. Marine and Freshwater
Behavior and Physiology.
35(1-2): 111-128.
Wenger, A. S., Fabricius,
K. E., Jones, G. P., and Brodie, J. E. (2015a). Effects of sedimentation, eutrophication, and chemical pollution on coral reeffishes. In C. Mora (Ed.), Ecology
of fishes on coral reefs (pp. 145-153). United
Kingdom: Cambridge University
Press.
Wenger, A. S., Williamson,
D. H., da-Silva, E. T., Ceccarelli, D. M., Browne, N. K., Petus, C., and Devlin, M. J. (2015b). Effects of
reduced water quality on coral reefs in and out of no-take marine reserves. Conservation
Biology. 30(1): 142-153.
Wilson,
S. K., Graham, N. A. J., Pratchett, M. S., Jones, G.
P., and Polunin, N. V. C. (2006). Multiple
disturbances and the global
degradation of coral reefs:
Are reef fishes at risk or resilient?
Global
Change Biology. 12:
2220-2234.
Zlatarsky, V. N. y Martínez-Estalella, N. (2018). Los escleractinios de Cuba con datos sobre sus organismos
asociados, Corpus Christi: Harte Research Institute for Gulf
of Mexico Studies at Texas
A&M University. 471 Pp.