Dinámica
temporal de la infestación por muérdago enano (Arceuthobium globosum y A.
vaginatum) en Zoquiapan (Parque Nacional
Popocatépetl), México
Temporal dynamics of dwarf mistletoe infestation
(Arceuthobium globosum and
A. vaginatum) in Zoquiapan
(Iztaccíhuatl Popocatépetl
National Park), Mexico
Mónica Elisa
Queijeiro-Bolaños* y Zenón Cano-Santana
Autor para
correspondencia: mqueijeiro@ciencias.unam.mx / Fecha de
recepción: 16 de enero de 2014/ Fecha de aceptación: 21 de enero de 2015.
Universidad
Nacional Autónoma de México. Facultad de Ciencias. Laboratorio de Interacciones
y Procesos Ecológicos. Departamento de Ecología y Recursos Naturales, Av.
Universidad 3000, D.F., México, C.P. 04510.
RESUMEN
Los
muérdagos enanos se encuentran entre los parásitos forestales que tienen mayor
impacto biológico y económico en los bosques templados; sin embargo, se sabe
poco acerca de la dinámica temporal de la infestación. El objetivo de este
trabajo fue conocer cómo cambia en el tiempo la incidencia de Arceuthobium vaginatum y A. globosum
sobre Pinus hartwegii en
la región de Zoquiapan, dentro del Parque Nacional
Iztaccíhuatl Popocatépetl, México. Durante dos años y medio (noviembre 2008 a
mayo 2011) se registró la incidencia de muérdago (proporción de árboles
infestados), la abundancia de hospederos y la abundancia de pinos menores a 2 m
en 24 parcelas de 3 300 m2. Se encontró que la infestación es altamente
variable entre fechas, especies y sitios, sin embargo, A. vaginatum mostró una mayor incidencia
que A. globosum
(Z = 44.09, P < 0.0001). Asimismo, la ocurrencia de incendios y la tala
parecen haber afectado la incidencia de los muérdagos, e incluso, en algunos
casos, se observaron rebrotes severos. La incidencia de A. vaginatum tuvo una correlación
negativa con la abundancia de pinos menores a 2 m (rs
= - 0.414, P < 0.05), por lo que esta especie pudo estar afectando el
reclutamiento de individuos juveniles, mientras A. globosum no mostró una correlación
significativa. Es necesario tomar en cuenta los sucesos estocásticos (como
incendios) en los planes de manejo del muérdago enano, para mejorar la
conservación de los recursos forestales.
PALABRAS CLAVE: muérdago enano, Pinus hartwegii, Zoquiapan, infestación, incidencia.
ABSTRACT
Dwarf mistletoes are forest parasites of great impact on temperate forests,
both at the biological and the economical level; however, little is known about the temporal dynamics of their infestation.
The aim of this study was to know how the incidences of Arceuthobium
vaginatum and A. globosum
change through time in the Zoquiapan region, inthe Iztaccíhuatl Popocatépetl National Park, Mexico. For two and a half
years (november 2008 to may 2011), it was registered
the incidence of dwarf mistletoe (proportion of infected trees), hosts
abundance, and the abundance of pines smaller than 2 m in height on 24 plots of
3 300 m2. It was found that infestation dynamics varies greatly,
between species and plots, and that A. vaginatum showed
a greater incidence than A. globo-sum (Z =
44.09, P < 0.000 1). Also, the occurrence of fires and logging apparently
affected the mistletoe incidence, and even, in some cases, mistletoe regrowth
was observed. The incidence of A. vaginatum had
a negative correlation with small pines abundance (rs
= - 0.414, P < 0.05), which could be indicating that there is a negative
effect on sapling recruitment. It is necessary to incorporate the occurrence of
stochastic phenomena (like fires) to dwarf mistletoe management programs, to
improve the conservation of forest resources.
KEYWORDS: dwarf mistletoe, Pinus hartwegii, Zoquiapan, infestation, incidence.
INTRODUCCIÓN
Los muérdagos enanos (Arceuthobium
spp., Santalales: Viscaceae)
son plantas hemiparásitas, que desarrollan una
estructura especializada llamada haustorio, por medio de la cual obtienen sus
nutrientes minerales, agua y parte de sus fotosintatos
(> 70 %) a partir del sistema vascular de su hospedero (Press
y Phoenix, 2005).
Esta
característica hace que los muérdagos enanos sean sujetos de estudio sumamente
interesantes, ya que afectan a árboles de interés forestal (Heide-Jorgensen, 2008; Rist y
col., 2008), aunado al hecho de que pueden mantener una asociación estrecha con
otros organismos, como aves, mamíferos y artrópodos (Watson y Herring, 2012). En México tienen una amplia distribución en
los bosques templados (Cibrián y col., 2007), parasitando particularmente
gimnospermas, considerándose al país como un centro de diversidad al presentar
21 especies del género (Hawksworth y Wiens, 1996; Mathiasen y col.,
2008).
A diferencia de otras especies de muérdago, que son
dispersados por aves (Aukema, 2003; Mathiasen y col., 2008), los muérdagos enanos tienen una
dispersión de tipo explosiva, en la cual las semillas son disparadas a gran
velocidad por el efecto de una presión hidrostática dentro del fruto (Hawksworth y Wiens, 1996). Si la
semilla alcanza un sitio seguro para la germinación, como son las ramas y
grietas de la corteza del fuste del hospedero, se desarrolla el apresorio, que es la estructura que penetra hacia los haces
vasculares del hospedero, y posteriormente comienza la formación del haustorio
y la conexión con el xilema (Musselman y Press, 1995; Hawksworth y Wiens, 1996). De forma que, para la propagación de la
infestación, es necesario que haya hospederos adecuados cercanos al árbol
fuente, y que éstos posean una copa amplia capaz de interceptar las semillas;
mientras que los eventos de intensificación de la infestación están dados por
la reinfección del hospedero (Shaw y col., 2005). Debido a que la distancia de
dispersión no supera los 14 m a 15 m (Robinson y Geils,
2006), y a que existen barreras físicas, como los árboles no susceptibles a la
infección (Shaw y col., 2005), es común que se creen zonas de infección donde los
muérdagos se concentran en pocos árboles vecinos.
Los muérdagos enanos pueden tener un impacto
imperceptible sobre el hospedero cuando la severidad (número de parásitos por
hospedero) es baja; sin embargo, cuando esta variable tiene valores altos, el
hospedero sufre un decremento en crecimiento, fecundidad y supervivencia (Press y Phoenix, 2005; Mathiasen
y col., 2008). Esto lleva a pérdidas significativas de aproximadamente 2
millones de m3 en la producción anual de madera en rollo a nivel
nacional.
Los
parques nacionales no están exentos de la infestación por muérdago enano, ya
que muchos de éstos concentran grandes masas de bosques templados. El Parque
Nacional Iztaccíhuatl Popocatépetl (PNIP), contemplando toda sus regiones,
comprende un gradiente altitudinal entre los 3 000 m y los 5 480 m, por lo que
es una zona geomorfológicamente compleja donde predominan los climas fríos
(DOF, 2013). Por la confluencia de las zonas biogeográficas neártica
y neotropical, presenta una gran diversidad biológica
donde dominan los bosques de coníferas de alta montaña, con una dominancia de Pinus hartwegii,
entre otras especies de gimnospermas (Rzedowski,
2006; DOF, 2013). En esta zona se encuentran dos especies de muérdago enano
parasitando a P. hartwegii: Arceuthobium globosum y
A. vaginatum, con incidencias entre el 3 % y
el 77 % por alguna de estas dos especies (Hernández-Benítez y col., 2005; Queijeiro-Bolaños y col., 2011; 2013). Aún más, existen
evidencias de que los disturbios antropogénicos como son los incendios, la
tala, la ganadería y los tiraderos de basura, afectan la incidencia de muérdago
en esta zona (Queijeiro-Bolaños y col., 2013).
A pesar de que se han realizado estudios acerca del
efecto del muérdago sobre el crecimiento del hospedero y su relación con la severidad de la infestación (Geils y Hawksworth, 2002), en
general existen pocos estudios sobre la infestación por Arceuthobium,
y en el caso particular de la dinámica de la infestación no se cuenta con
trabajos al respecto. En México se han realizado principalmente estudios sobre
el estado sanitario en los bosques templados, además del reconocimiento de las
variables que influyen sobre la infestación (Musalem
y Solís, 2000; Ramírez-Dávila y Porcayo-Camargo,
2010; Clark-Tapia y col., 2011). Para el PNIP, se ha registrado que la
infestación está asociada positivamente a la altura y la cobertura de los
pinos (Arriaga y col., 1988; Hernández-Benítez y col., 2005), además de que se
asocia a las características topológicas de los sitios, como la altitud y la
pendiente (Queijeiro-Bolaños y col., 2013), y que la
infestación muestra ciertos patrones de agregación (Queijeiro-Bolaños
y col., 2014). Debido a lo anterior, el objetivo del presente trabajo fue
establecer cómo cambia la infestación de dos especies de muérdago enano, A. globosum y A. vaginatum,
a través del tiempo, en rodales de P. hartwegii dentro
del PNIP.
MATERIALES Y MÉTODOS
Sitios y especies de estudio
El estudio se llevó a cabo dentro del Parque Nacional
Iztaccíhuatl Popocatépetl (PNIP; Figura 1) en la región que corresponde a Zoquiapan y el Papayo, Estado de México (19°15-29” N, 98°37-45’
O, 3 200 msnm a 3438 msnm). La vegetación se compone principalmente por
bosques de P. hartwegii y Abies
religiosa, aunque también se pueden encontrar bosques mixtos de P. hartwegii con otras especies de Pinus,
Quercus, Cupressus, Abies y Alnus. El
sotobosque está representado principalmente por pastos zacatonales
como Muhlenbergi robusta y Festuca spp.;
además de arbustos, como Senecio spp. y Eupatorium spp., y hierbas, como Lupinus
spp. (Obieta y Sarukhán, 1981; DOF, 2013). El clima es templado subhúmedo
con lluvias en verano; la temperatura media anual es de 9.7 °C y la
precipitación anual de 941 mm, con las lluvias concentradas de junio a septiembre
(SMN, 2013).

En esta zona, P. hartwegii es parasitado
por Arceuthobium globosum Hawksworth y Wiens subsp. grandicaule Hawksworth y Wiens y Arceuthobium vaginatum (Willdenow) Presl subsp vaginatum (Figura
2) (Queijeiro-Bolaños y col., 2013). A. globosum es un arbusto que mide de 18 cm a 70 cm de largo,
sus tallos son de color amarillo verdoso; presenta una antesis entre marzo y
abril, y fructifica en agosto. A. vaginatum mide
de 20 cm a 55 cm de largo, sus tallos son de color pardo o negro, tiene una antesis de enero a mayo, y fructifica de julio a
noviembre (Hawksworth y Wiens,
1996; Cibrián y col., 2007).

Obtención de datos
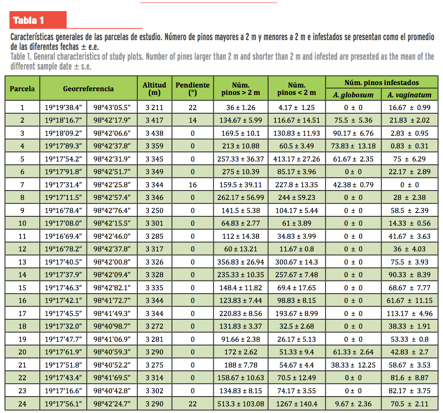
Se seleccionaron 24 parcelas permanentes de 60 m x 55
m, que tuvieran una clara dominancia de Pinus
hartwegii (Tabla 1). Se consideró que 24
parcelas de 3 300 m2 son una muestra representativa y manejable para
realizar censos en distintas
fechas. Dentro de cada parcela se muestrearon cuatro transectos
de 60 m × 10 m, método comúnmente usado en censos forestales (Muir y Moody, 2002), dejando 5 m de separación entre sí. En cada transecto se tomaron los siguientes datos cada seis meses,
por dos años y medio (noviembre 2008 a mayo 2011): total de individuos de P.
hartwegii mayores y menores a 2 m, número de
árboles infestados por A. globosum o por A.
vaginatum, y número de árboles no hospederos.
Debido a que los individuos de P. hartwegii menores
a 2 m tienen una baja probabilidad de ser infestados (Hernández-Benítez y col.,
2005), sólo se contabilizó la infestación en los individuos mayores a dicha
talla. A pesar de que un solo árbol puede presentar co-infestación
por las dos especies, se contabilizó de manera individual cada especie para
cumplir con el objetivo de conocer la dinámica para cada una.
Análisis de datos
Se calculó la incidencia (proporción de individuos infestados) de A. globosum y de A. vaginatum
en cada parcela, para cada una de las fechas de muestreo. Asimismo, se
calculó la incidencia promedio de cada especie para cada fecha de muestreo y se
obtuvo la incidencia general que incluye todas las fechas en conjunto. Para
explorar las diferencias entre las proporciones de árboles infestados por cada especie de
muérdago, se realizó una prueba de hipótesis para la diferencia entre dos
proporciones (Z), tanto para cada temporada, como para todo el período en
conjunto. Al tratarse de datos no independientes, se aplicó la corrección de Bonferroni, donde el nivel de significancia se ajusta como
α/n, donde n se refiere al número de comparaciones realizadas (Zar, 2010).
Adicionalmente, para saber si hay relación entre la infestación por muérdago y
el reclutamiento de árboles juveniles, se hizo una correlación de Spearman (rs), entre el
porcentaje de árboles infestados por cada especie de muérdago y la abundancia
de pinos menores a 2 m.
RESULTADOS
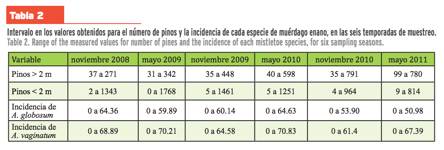
La incidencia de las dos especies de muérdago enano fue sumamente variable
entre parcelas y fechas de muestreo; sólo una parcela estuvo libre de
infestación, mientras que en el resto se encontró a A.
vaginatum; y A. globosum
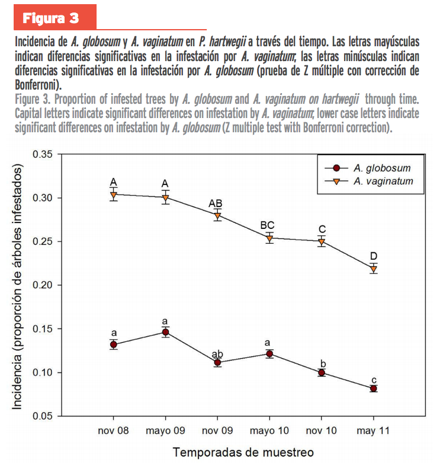
sólo se presentó en nueve de éstas (Tablas 1 y 2). A. vaginatum disminuyó su incidencia a lo largo del
tiempo (de 0.30 a 0.22; Figura 3), mientras que A. globosum
tuvo una temporada donde su incidencia se incrementó (noviembre 2008 a mayo
2009); sin embargo, ésta decreció durante el último año de muestreo (mayo 2010
a mayo 2011; Figura 3). En la incidencia promedio, considerando todas las temporadas y parcelas, fue
siempre significativamente mayor la de A. vaginatum
que la de A. globosum (Z = 44.09, P <
0.0001).
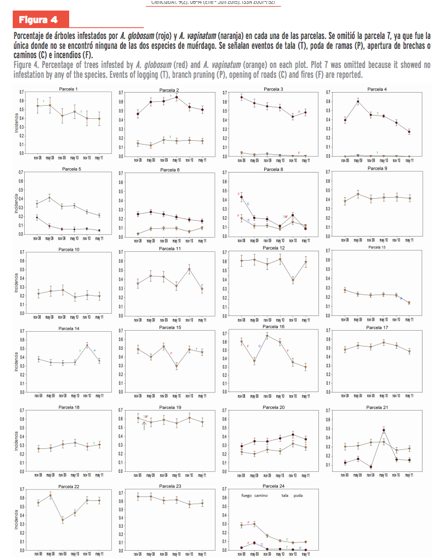
No se observa un patrón general de crecimiento o decrecimiento de la
incidencia para cada parcela individual; aparentemente los cambios están
influidos por procesos estocásticos, tales como incendios y/o tala, los cuales
fueron eventos inesperados durante el transcurso de la investigación (Figura
4). Aunque no es posible distinguir una tendencia general en cuanto a estos
disturbios, en la mayoría de los casos, donde la incidencia decrece, se asocia
a un evento de tala de pinos, ya sea remoción de árboles, poda de ramas o apertura
de brechas/caminos (Figura 4).
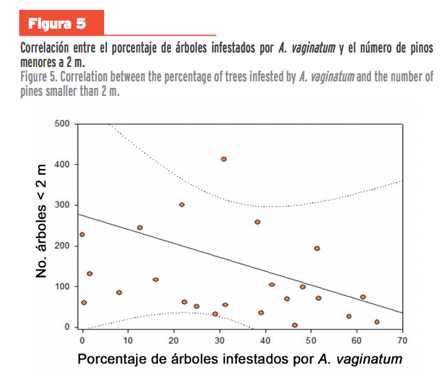
La frecuencia de pinos por parcela, tanto de individuos menores como
mayores a 2 m, fluctuó a lo largo del tiempo. El porcentaje de árboles
infectados por A. globosum no presentó una
correlación significativa con el número de árboles menores a 2 m (rs = 0.196, P > 0.05); en cambio, el porcentaje de
árboles infestados por A. vaginatum presentó
una correlación significativa y negativa con la frecuencia de árboles menores a
2 m (rs = - 0.414, P < 0.05; Figura 5).
DISCUSIÓN
La incidencia de A. vaginatum
pareció disminuir, mientras que la de A. globosum
creció o decreció según la emporada en el periodo de estudio; puede ser una
respuesta a eventos estocásticos propios de la dinámica del bosque, debido a
sucesos naturales (incendios) o antropogénicos (remoción de árboles, poda de
ramas y apertura de nuevos caminos, así como incendios provocados). Esto
sugiere que los muérdagos enanos representan un sistema muy variable y que son
sensibles a las fluctuaciones de las actividades antropogénicas. Asimismo,
revela que en general la incidencia no se está incrementando, por lo cual no
representarían una amenaza para los recursos forestales de esta zona, al menos
por el momento. Más aún, las incidencias de estas especies de muérdago están
dentro del intervalo reportado para éstas y otras especies, que va desde
1.8 % hasta 77 % (Hernández-Benítez y col., 2005;
Ramírez-Dávila y Porcayo-Camargo, 2010; Sarangzai y col., 2010), mostrando que la infestación
sigue el mismo patrón.
Existe poca información científica sobre la fluctuación temporal de la
incidencia de especies de muérdago y, en específico de muérdago enano (Arceuthobium globosum y
A. vaginatum). Reid
y Smith (2000), monitorearon la dinámica de Amyema
preissii en el norte de Australia por cinco
años, durante los cuales observaron fluctuaciones en la infestación entre 11 %
y 46 %; sin embargo, esto sucedió después de un tratamiento de remoción de
muérdago, y los árboles presentaron una tasa de reinfección, lo que señala que
la infestación por muérdago puede ser muy dinámica a corto plazo.
Se sabe que los muérdagos en general (Loranthaceae
y Viscaceae), responden a las presiones ambientales
(Hawksworth y Wiens, 1996; Mathiasen y col., 2008). Algunos estudios reportan que el
muérdago tiende a incrementar su abundancia con el disturbio antropogénico, y
generalmente están enfocados a que la fragmentación deja pocos sitios de percha
y anidación para aves dispersoras de muérdago, ocasionando la formación de centros de infección en
los árboles remanentes (Burguess y col., 2006; Kelly
y col., 2008; Bowen y col., 2009; MacRaild
y col., 2010). Aunque no está claro aún para el caso de la tala, se ha visto
que la disminución en la densidad de hospederos puede favorecer la infestación
en los árboles remanentes (Donohue, 1995; Queijeiro-Bolaños y col., 2013), ya que los muérdagos
reciben una mayor incidencia de luz, la cual es necesariaparalaproducción
de estructuras vegetativas y reproductivas, además que se aumenta la
probabilidad de infestación en los árboles remanentes (Bickford
y col., 2005). Además, los pinos hospederos experimentan menos competencia por
recursos al tener una menor cantidad de árboles vecinos, derivando por lo
tanto, una mayor cantidad de recursos
hacia las hemiparásitas (Bickford
y col., 2005). En el otro extremo, la poda desmedida no sólo puede reducir la
infestación sino que afecta el desempeño de los hospederos (Endara-Agramont y col., 2012).
En el presente estudio, la presencia de incendios parece haber afectado
también la incidencia de muérdago enano. Se ha reportado que los incendios
controlados pueden ser una forma de manejo efectiva del muérdago enano (Kipfmueller y Baker, 1998), ya que los hospederos son resistentes
a los incendios, mientras que los muérdagos son muy sensibles a éstos (Kipfmueller y Baker, 1998; Rodríguez-Trejo y col., 2004).
Sin embargo, las evidencias de otros estudios son contradictorias. Por
ejemplo, Hessburg y col. (2008), sostienen que tratamientos
experimentales de aclareo e incendios prescritos no disminuyeron la severidad del muérdago de manera
significativa. Como se puede ver en este estudio, en algunas parcelas, después
de los incendios, la incidencia decreció. Más aún, la relación entre muérdagos
e incendios es compleja, ya que las hemiparásitas
afectan la cantidad y tipo de material combustible en el bosque, al incrementar
la cantidad de material inflamable (Stanton y Hadley, 2010).
En este estudio, tanto la tala como los incendios se presentaron en
temporadas seguidas o incluso en la misma temporada, lo que afectó en gran
medida la incidencia. Aunque en las parcelas estudiadas no se observó algún
efecto negativo de los disturbios sobre la mortalidad de los hospederos, se
sabe que si éstos son muy intensos pueden diezmar las poblaciones de pinos
(DOF, 2013). Se ha reportado, por ejemplo, que en la zona ha disminuido la
cobertura vegetal en un 30 %, debido a la tala y otros factores (DOF, 2013), lo
cual puede tener
como consecuencias a futuro, el cambio en la incidencia de muérdago enano,
además de que tiene efectos negativos sobre las poblaciones de P. hartwegii. Aunque existen evidencias previas de que la
tala y los incendios tienen una fuerte influencia sobre la incidencia de estas
dos especies de muérdago enano (Queijeiro-Bolaños y
col., 2013), y al parecer influyen sobre las fluctuaciones temporales, es
necesario dirigir esfuerzos experimentales para conocer el efecto del disturbio
a lo largo del tiempo.
El número de individuos de P.hartwegii,
en este caso, fluctuó a través del tiempo. En otros estudios se ha visto
que se debe a la mortalidad de los hospederos, ya sea por la infección o por
otras causas naturales (Reid y Smith, 2000); sin
embargo, en el presente estudio se debió a la remoción o crecimiento de los
árboles: cuando la frecuencia de árboles > 2 m decreció, fue debido a la
tala y la apertura de caminos. En cambio, el aumento en el número de estos
árboles, tal vez se daba por el crecimiento de los árboles menores que ya alcanzaban una talla mayor a los
2 m. Asimismo, el incremento en árboles pequeños pudo deberse al reclutamiento
de nuevos individuos. La presencia de A. globosum no
está correlacionada con el número de árboles menores a 2m; sin embargo, A. vaginatum si lo está, lo que puede ser un indicador de
que en los rodales infestados por esta especie hay un menor reclutamiento de
individuos juveniles y que su parasitismo sí tiene efectos sobre la fecundidad
del hospedero. Es sabido que la infección de muérdago enano reduce el éxito
reproductivo de los hospederos, ya que la producción de conos y semillas es
afectada, por lo tanto disminuye el reclutamiento (Geils
y Hawksworth, 2002). Sin embargo, se necesitan más
estudios dirigidos a conocer el efecto del parasitismo por A. vaginatum sobre la fecundidad y la adecuación de P. hartwegii. Cabe señalar que la tala y la poda no fue
dirigida a los individuos de esta talla.
CONCLUSIONES
La infestación
por muérdago enano dentro del Parque Nacional Iztaccíhuatl Popocatépetl (PNIP),
no representarían actualmente una amenaza para los rodales de P. hartwegii, ya que la incidencia de la infestación, al
menos para el período de estudio, no se incrementó, y las poblaciones de
muérdago son reguladas por la dinámica y perturbaciones del bosque. Sin
embargo, debe tomarse en cuenta que el disturbio antropogénico puede modificar
la infestación, favoreciendo una mayor incidencia y rebrotes severos posteriores.
Esto debe ser tomado en cuenta para los planes de manejo y saneamiento forestal
dentro del PNIP, para una mejor conservación de sus recursos.
REFERENCIAS
Arriaga, L., Franco, M., and Sarukhán, J. (1988). Identification of natural groups of
trees in uneven-aged forests using multivariate methods. Journal of Ecology. 76:
1092–1100.
Aukema, J. E. (2003). Vectors, viscin, and Viscaceae: mistletoes
as parasites, mutualists, and resources. Frontiers in
Ecology and the Environment. 1(3): 212–219.
Bickford, C. P., Kolb, T. E., and Geils,
B. W. (2005). Host physiological condition regulates parasitic plant
performance: Arceuthobium vaginatum
subsp. cryptopodum on Pinus
ponderosa. Oecologia. 146(2):
179–189.
Bowen, M. E., McAlpine, C. A.,
House, A. P. N., and Smith, G. C. (2009). Agricultural landscape modification
increases the abundance of an important food resource: mistletoes, birds and brigalow. Biological Conservation. 142: 122–133.
Burguess, V. J., Kelly, D.,
Robertson, A. W., and Ladley, J. J. (2006). Positive effects of forest edges on
plant reproduction: literature review and a case study of bee visitation to
flowers of Peraxilla tetrapetala
(Loranthaceae). New Zealand
Journal of Ecology. 30: 179–190.
Cibrián, D., Vázquez, I. y Cibrián, J. (2007). Muérdagos enanos del género Arceuthobium.
En D. Cibrián, D. Alvarado y S. García (Eds.), Enfermedades forestales
en México (pp. 357–395). Montecillo, Estado de México, México: Universidad
Autónoma de Chapingo.
Clark-Tapia, R.,
Torres-Bautista, B., Alfonso-Corrado, C., Valdez-Hernández, J., González-Adame,
G., Bretado-Velásquez, J. y Campos-Contreras, J. (2011). Análisis de la
abundacia y la infección por muérdago en Sierra Fría, Aguascalientes, México. Madera
y Bosques. 17(2): 19-33.
DOF, Diario
Oficial de la Federación (2013). Acuerdo por el cual se da a conocer el resumen
del Programa de Manejo del Parque Nacional Izatccíhuatl Popocatépetl. [En
línea]. Disponible en:
http://dof.gob.mx/nota_detalle.php?codigo=5294188&fecha=02/04/2013. Fecha
de consulta: 5 de septiembre de 2013.
Donohue, K.
(1995). The spatial demography of mistletoe parasitism on a Yemeni Acacia. International
Journal of Plant Sciences. 156(6): 816–823.
Endara-Agramont, A. R., Franco-Maass, S., Nava-Bernal, G., Valdez-Hernández, J. I., and Fredericksen, T. S. (2012). Effect of human disturbance on the structure and regeneration of forests in the Nevado de Toluca National Park, Mexico. Journal of Forestry Research. 23(1): 39–44.
Geils, B. W. and Hawksworth,
F. G. (2002). Damage, Effects, and Importance of Dwarf
Mistletoes. En B. W. Geils, J. Cibrián-Tovar, and B. Moody (Eds.), Mistletoes of North
American Conifers (pp. 57–66). Ogden, EUA: USDA Forest Service General
Technical Report.
Hawksworth, F. G. and Wiens, D. (1996). Dwarf
Mistletoes: Biology, Pathology, and Systematics.Washington, D.C: USDA Forest
Service. 410 Pp.
Heide-Jorgensen, H. (2008). Parasitic flowering plants. Leiden, Holanda. Brill. 438 Pp.
Hernández-Benítez,
R., Cano-Santana, Z. y Castellanos-Vargas, I. (2005). Incidencia de infestación
de Arceuthobium globosum grandicaule (Hawks y Wiens) en Pinus
hartwegii (Lindl.). Ciencia Forestal en México. 30: 79–86.
Hessburg, P. F.,
Povak, N. A., and Salter, R. B. (2008). Thinning and prescribed fire effects on dwarf
mistletoe severity in an eastern Cascade Range dry forest, Washington. Forest
Ecology and Management. 255(7): 2907–2915.
Kelly, D., Ladley, J. J.,
Robertson, A. W., and Crowfoot, L. (2008). Flower predation by Zelleria maculate (Lepidoptera) on Peraxilla
mistletoes: effects of latitude and fragmentation, an impact on fruit set. New Zealand Journal of Ecology. 32:
186–196.
Kipfmueller, K. and Baker, W. (1998). Fires and dwarf mistletoe in a Rocky Mountain lodgepole pine ecosystem. Forest Ecology and Management. 108: 77–84.
MacRaild, L. M., Radford, J. Q., and Bennet,
A. F. (2010). Non-linear effects of landscape properties on
mistletoes parasitism in fragmented agricultural landscapes. Landscape
Ecology. 25: 395–406.
Mathiasen, R. L., Shaw, D. C., Nickrent, D., and Watson, D. (2008). Mistletoes. Pathology,
Systematics, Ecology, and Management. Plant Disease. 92(7): 988–1006.
Muir, J. A. and Moody, B. (2002). Dwarf mistletoe
surveys. En B. W. Geils, J. Cibrián-Tovar,
and B. Moody (Eds.), Mistletoes of North American Conifers (pp. 67–74).
Ogden, EUA: USDA Forest Service General Technical Report.
Musálem S. M. A.
y Solís M. A. (2000). Monografía de Pinus hartwegii. Chapingo, México:
Secretaría de Agricultura, Ganadería y Desarrollo Rural, Instituto Nacional de
Investigaciones Forestales, Agrícolas y Pecuarias, Centro de Investigación
Regional del Centro-Campo Experimental Valle de México. 96 Pp.
Musselman, L. and Press, M. (1995). Introduction to parasitic plants. En M. Press y J. Graves
(Eds.), Parasitic plants (pp. 1–13). Londres,
RU: Chapman and Hall.
Obieta, C. y
Sarukhán, J. (1981). Estructura y composición de la vegetación herbácea de un
bosque uniespecífico de Pinus hartwegii: 1. Estructura y composición
florística. Boletín de la Sociedad Botánica Mexicana. 41: 75–125.
Press, M. C. and Phoenix, G. K. (2005). Impacts of parasitic plants on natural communities. The
New Phytologist. 166(3): 737–751.
Queijeiro-Bolaños,
M. E., Cano-Santana, Z. y Castellanos-Vargas, I. (2011). Distribución
diferencial de dos especies de muérdago enano sobre Pinus hartwegii en
el área natural protegida “Zoquiapan y anexas”, Estado de México. Acta
Botanica Mexicana. 96: 49–57.
Queijeiro-Bolaños,
M. E., Cano-Santana, Z. and Castellanos-Vargas, I. (2013). Does disturbance determines the
prevalence of dwarf mistletoe (Arceuthobium, Santalales:Viscaceae) in Central
Mexico?. Revista Chilena de Historia Natural.
86: 181–190.
Queijeiro-Bolaños,
M. E., Cano-Santana, Z., and García Guzmán, G. (2014). Incidence, severity, and
aggregation patterns of two sympatric dwar mistletoe
species (Arceuthobium spp.) in Central
Mexico. European
Journal of Forest Research. 113(2): 297-306.
Ramírez-Dávila,
J. F. y Porcayo-Camargo, E. (2010). Estudio comparativo de la distribución
espacial del muérdago enano (Arceuthobium sp.) en la ladera norte del
Parque Nacional Nevado de Toluca, México. Bosque. 31(1): 28–38.
Reid, N. and Smith, M. S. (2000). Population dynamics
of an arid zone mistletoe (Amyema preissii, Loranthaceae) and
its host Acacia victoriae (Mimosaceae).
Australian Journal of Botany. 48: 45–58.
Rist, L., Shaanker,
R. U., Milner-Gulland, E. J., and Ghazoul, J. (2008).
Managing mistletoes: The value of local practices for a non-timber forest
resource. Forest Ecology and Management. 255(5-6):
1684–1691.
Robinson, D. C. E. and Geils, B. W. (2006). Modelling dwarf mistletoe at
three scales: life history, ballistics and contagion. Ecological
Modelling. 199(1): 23–38.
Rodríguez-Trejo, D.
A., Martínez-Hernández, H. C. y Ortega-Baranda, V. (2004). Ecología del fuego
en bosques de Pinus hartwegii. En L. Villers-Ruiz y J. López-Blanco. Incendios
forestales en México. Métodos de evaluación (pp. 103–120). México, D.F.,
México: Universidad Nacional Autónoma de México.
Rzedowski, J.
(2006). Vegetación de México. Distrito Federal, México: Comisión Nacional para
el Conocimiento y Uso de la Biodiversidad. [En línea]. Disponible en:
http://www.biodiversidad.gob.mx/publicaciones/librosDig/pdf/VegetacionMx_Cont.pdf.
Fecha de consulta: 3 de octubre de 2012.
Sarangzai, A. M., Khan, N., Wahab, M., and Kakar, A. (2010). New spread of dwarf mistletoe (Arceuthobium oxycedri) in
juniper forests, Ziarat, Balochistan,
Pakistan. Pakistani Journal of Botany. 42(6): 3709–3714.
Shaw, D. C., Chen, J., Freeman, E.
A., and Braun, D. M. (2005). Spatial and population characteristics of dwarf
mistletoe infected trees in an old-growth Douglas-fir western hemlock forest. Canadian
Journal of Forest Research. 35: 990–1001.
SMN, Servicio
Meteorológico Nacional. (2013). Normales climatológicas. [En línea]. Disponible
en: http://smn.cna.gob.mx/. Fecha de consulta: 2 de junio de 2013.
Stanton, S. and Hadley, K. S. (2010). Influence of
western dwarf mistletoe (Arceuthobium campylopodum Engelm.) on
surface fuels and snag abundance in mature ponderosa pine and mixed conifer
stands in central Oregon. Natural Areas Journal.
30(3): 261–270.
Watson, D. M. and Herring, M. (2012). Mistletoe as a
keystone resource: an experimental test. Proceedings of
the Royal Society. 279: 3853–3860.
Zar, J. (2010). Biostatistical
analysis. New Jersey, EUA: Prentice Hall. 944 Pp.