Efecto
prebiótico de los Arabinoxilanos y los Arabinoxilo-Oligosacáridos y su relación
con la promoción de la buena salud
Prebiotic
effect of Arabinoxylans and Arabinoxylan-Oligosaccharides and the relationship
with good health promotion
Jorge Marquez-Escalante1*, Elizabeth Carvajal-Millan1, Yolanda L. López-Franco1, Elisa M. Valenzuela-Soto2, Agustín Rascón-Chu3
*Correspondencia: marquez1jorge@gmail.com/
Fecha de recepción: 29 de marzo de 2017/ Fecha de aceptación: 10
de julio de 2017
1Centro
de Investigación en Alimentación y Desarrollo, A.C., Coordinación de Tecnología
de Origen Animal, carretera a La Victoria Km 0.6, Hermosillo, Sonora, México,
C.P. 83304. 2Centro de
Investigación en Alimentación y Desarrollo, A.C., Coordinación de Ciencias de
los Alimentos. 3Centro de
Investigación en Alimentación y Desarrollo, A.C., Coordinación de Tecnología de
Alimentos de Origen Vegetal.
RESUMEN
Los arabinoxilanos son polisacáridos presentes
en los granos de los cereales, y como tales, forman parte de la fibra dietética
consumida por humanos y animales. La hidrólisis química o enzimática de los
arabinoxilanos produce arabinoxilo-oligosacáridos, los cuales pueden estar ramificados o no, con arabinosa. El objetivo de
este trabajo fue exponer el uso potencial de los
arabinoxilanos y arabinoxilo-oligosacáridos, como
prebióticos, y el efecto de su consumo en la promoción de la buena
salud, al estimular selectivamente el crecimiento y actividad metabólica de la
microbiótica colónica benéfica. La información generada indica que los arabinoxilanos
y arabinoxilo-oligosacáridos actúan modificando la microbiota de manera
selectiva, y estimulan la respuesta biológica, favoreciendo la buena salud del
hospedero, por su efecto antiobesogénico, regulador de la glucosa, antioxidante,
anticancerígeno e inmunomodulador, con resultados similares o mejores en
relación a prebióticos reconocidos. No obstante, es necesario ampliar el
conocimiento que se tiene de ellos para sustentar su aplicación en la industria
alimentaria, farmacéutica o biomédica.
PALABRAS
CLAVE: cereales, polisacáridos, oligosacáridos,
prebióticos, probióticos.
ABSTRACT
Arabinoxylans
are polysaccharides present in grains and as such, are part of dietary fiber intake in humans and animals. Enzymatic or chemical
hydrolysis of arabinoxylans produces arabinoxilo-oligosaccharides, which can be branched or unbranched with arabinose. The objective
of this work was to describe the potential use of arabinoxylans and
arabinoxylan-oligosaccharides as prebiotics
to promote good health, by selective enhancement of beneficial colonic
microbiota growth and metabolic activity. The
information generated indicates that arabinoxylans and
arabinoxylan-oligosaccharides act by modifying the microbiota selectively and
stimulate the biological response favoring good health in the host, by
antio-obesity effect, glucose regulator, antioxidant, anticancer, immunomodulator,
with similar or better results than recognized prebiotics. However, it is
necessary to expand the knowledge we have about arabinoxylans in order to
support their application in the food, pharmaceutical, and biomedical industry.
Keywords: cereals, polysaccharides,
oligosaccharide, prebiotics, probiotics.
INTRODUCCIÓN
Los cereales han representado un alimento nutritivo básico
en la dieta de la humanidad a través de su historia, y recientemente, los
avances científicos han demostrado bondades adicionales en la promoción de la
buena salud, asociadas al consumo de estos alimentos (Birkett y Cho, 2013;
Jones y col., 2015). En concordancia, la producción de los dos cereales de
mayor consumo en México, el maíz y el trigo, se incrementó en un 2.7 % y 9.3 %,
respectivamente, del año 2013 al 2014 (FAO,
2017).
Estudios en humanos, han reportado que la ingestión de fibra dietética reduce el riesgo a padecer
enfermedades crónicas y degenerativas (Asp y col., 1993), las
cuales en 2015, generaron la muerte de 40 millones de personas (WHO, 2017). Dichas enfermedades se han incrementado
debido a que la población se ha sometido a un ritmo de vida caracterizado por altos niveles de estrés, consumo de
alimentos de bajo valor nutrimental (Patel y
Goyal, 2012) y un estilo de vida más
sedentario (Kirchengast, 2014).
Muchos de los efectos benéficos se han adjudicado a los
polisacáridos de la pared celular vegetal, tales como los arabinoxilanos (AX),
así como para algunos de sus derivados como los
arabinoxilo-oligosacáridos (AXOS) (Swennen y
col., 2006). Desde 2003, se ha acrecentado
el interés por estos polisacáridos, ya que se ha demostrado que pueden ser
considerados como prebióticos (Femia y col., 2010), por lo que podrían reducir
la incidencia de enfermedades como la neoplasia, la obesidad crónica, desórdenes gastrointestinales, diabetes, enfermedades coronarias, enfermedades degenerativas
y cáncer (Patel y Goyal, 2012).
El objetivo de este trabajo fue describir el
uso potencial de los arabinoxilanos (AX) y los arabinoxilo-oligosacáridos (AXOS) como prebióticos, y el efecto de su consumo en la promoción de la buena salud,
al estimular selectivamente el crecimiento y actividad de bacterias benéficas.
Origen
y estructura química de los AX y los AXOS
Los AX son polisacáridos que están presentes
en los granos de los cereales, localizándose en el endospermo, la aleurona, la
cutícula y el pericarpio, denominándose a
estos tres últimos en forma genérica como salvado (Izydorczyk y Billiaderis, 2007). Estos polisacáridos
están conformados por una cadena lineal de
miles de unidades de xilosa, unidas mediante enlaces β(1-4)
y ramificaciones con sustituyentes de arabinosa a través de enlaces en O-2 y/o
O-3 (Fincher y Stone, 1974) (Figura 1a). Al número de unidades presentes en las cadenas del polisacárido se le conoce como grado de polimerización
(GP), mientras que la relación entre la arabinosa y la xilosa se expresa como
grado de sustitución (GS). Otros sustituyentes de menor frecuencia son el ácido
glucurónico, la galactosa y los grupos acetilo
(Saulnier y col., 2007). Asimismo, algunos sustituyentes de arabinosa
tienen residuos esterificados de ácido
ferúlico en posición O-5 (Smith y Hartley, 1983). Los AX pueden ser
solubles en agua (WEAX, por sus siglas en inglés: water extractable
arabinoxilanos) e insolubles en agua (WUAX, por sus siglas en inglés: water
unextractable arabinoxilanos) (Izydorczyk
y Billiaderis, 2007).

Los AXOS son cadenas cortas de unidades de xilosa
sustituidas con unidades de arabinosa, las cuales pueden estar esterificadas a
ácido ferúlico, que se producen por degradación de los AX (Figuras 1a, 1b). La
hidrólisis de los AX y los AXOS puede llevarse a cabo durante el procesamiento de los cereales, para
transformarlos en productos alimenticios, debido a la presencia de enzimas endógenas que los degradan. Los AX y AXOS que
permanecen en los alimentos
pueden ser hidrolizados en el colon de los
animales y humanos, por efecto de la microbiota
endógena o natural, que produce enzimas como endo-β-D-xilanasa, β-D-xilosidasa, a-L-arabinofuranosida-d3,
a-L-arabinofuranosida-m y
feruloil esterasa. La endo-β-D-xilanasa rompe de manera aleatoria los enlaces
glucosídicos interiores de la cadena lineal de
unidades de xilosa y la β-D-xilosidasa
corta el enlace glucosídico de la unidad terminal de xilosa (Figura 1a). Por su
parte, las a-L-arabinofuranosidasas hidrolizan
los enlaces de ramificación entre las unidades de xilosa y arabinosa. En contraste, las feruloil esterasas cortan
los enlaces entre las unidades de arabinosa y ácido ferúlico. El resultado de
la actividad enzimática en conjunto produce
la disminución del peso molecular (PM) de los AX, produciendo AXOS y
xilo-oligosacáridos, y finalmente monosacáridos (Figura 1b)
(Grootaerty col., 2007).
Existen procesos de purificación de AX y
AXOS, a partir de fuentes con alto contenido
de AX, para que puedan ser utilizados como
ingredientes alimenticios, con el fin de modificar
alguna característica o incrementar el nivel de fibra. Estos procesos combinan
dos pasos: el primero es la solubilización en agua o solubilización
inducida por hidrólisis alcalina; y el segundo, por una hidrólisis que puede ser enzimática
o por condiciones de alta temperatura
y presión (Broekaert
y col., 2011).
Las
características estructurales que definen a los AXOS son el GP, GS y el
contenido de ácido ferúlico. El ácido glucurónico, también se ha detectado como componente minoritario del oligosacárido.
Los valores del GP y del GS de los AXOS reportados varían de 3 a 67 y de 0.09 a 0.58, respectivamente (Sanchez y col., 2009; Femia
y col., 2010).
AX y
AXOS en productos
de harina
El hecho
de que los AX y AXOS sean parte de los mayores componentes en los subproductos del procesamiento de los granos de cereales
(fibra o salvado de maíz, salvado de trigo, fibra de arroz, entre otros) o residuos agrícolas (rastrojo de maíz, paja
de trigo, bagazo de caña de azúcar, entre otros), ha permitido que estos polisacáridos tengan una aplicación potencial
en la industria alimenticia, con el fin de
obtener
productos con valor agregado (Yadav y Hicks, 2018). En específico, los AX han
sido estudiados de manera extensiva por el papel que desempeñan en el proceso
de panificación y su efecto en el producto
final. El uso de WEAX ofrece
beneficios tecnológicos en la panificación, como el incrementar la
consistencia y prevenir la coalescencia de
la masa, por lo que aumentan el volumen del pan y mejoran la textura de la miga (Izydorczyk y Biliaderis, 2007). Por
el contrario, los WUAX desestabilizan la estructura de la masa, disminuyen
el volumen del pan y producen una miga más dura y gruesa (Courtin y Delcour, 2002). Sin embargo, estos efectos negativos
se pueden disminuir o eliminar, al agregar enzimas endo-β-D-xilanasas, las cuales convierten los WUAX a WEAX de alto PM, mejorando la consistencia de la masa, la estabilización de la fermentación, el volumen del pan y la estructura y suavidad de la miga (Rouau y col.,
1994; Courtin
y Delcour, 2002). La enzima xilanasa
permitió obtener pan de centeno con una mejor calidad (volumen, dureza y
densidad) respecto al control. Estos
atributos se realzaron cuando en la fórmula de la masa, también se agregó
salvado de centeno (Döring y col.,
2017a) o la enzima transglutaminasa, que generó proteínas insolubles, al
reticular gluteninas de alto peso molecular
(Grossman y col., 2016; Döring y col., 2017b). En pan de trigo, el uso de una mezcla enzimática (0.25 %;
xilanasa, amilasa y celulasa) y la substitución del 20 % de harina de trigo por AX de salvado prefermentados, generaron
AX más solubles en la masa, permitiendo una mayor distribución de agua y en consecuencia un pan, con una calidad
superior al pan elaborado con 100 %
harina de trigo
suave (Messia y
col., 2016).
La
evaluación de productos de panadería enriquecidos con AX, ha puesto de
manifiesto el reto de crear alimentos que converjan en valor nutrimental y
atractivo para el consumidor. Por ejemplo, Lu y col. (2000), evaluaron pan
adicionado con un 7 % y 14 % de fibra (principalmente
conformada por AX), observando que la palatabilidad del producto es igual a la de pan con un 50 % de trigo entero.
A su vez, Koegelenberg y Chimphango (2017), observaron que una dosis del 0.8 %
de AX de salvado de trigo desplazó al 2.5 % de la harina, sin afectar los atributos físicos de pan, excepto el
color, manteniendo así el peso del pan, altura y volumen. En cambio, en pan libre
de gluten, se requirió adicionar 6 % de AX de
fibra de maíz para obtener un volumen específico más alto y una textura
de miga más suave (Ayala-Soto
y col., 2017).
Saeed y
col. (2015), elaboraron panes con AX de diferentes variedades de trigo y
proporciones (0.5 % y 1.0 %). La inclusión de los AX, al pan, proporcionó una
mejor consistencia, fracturabilidad y gomosidad, sin embargo, dichos atributos
disminuyeron durante su almacenamiento (6 d a 25 °C). En cambio, en otro
estudio, la adición de AX de salvado de centeno en masa y almacenada durante 60
d a - 18 °C, permitió obtener pan, con
características de textura y volumen de miga superiores al pan sin AX
adicionados (Wang y col., 2016). Este resultado se explicó en términos de una
menor cristalización del agua, debido
a la absorción que ejercen los AX,
manteniendo la viabilidad y actividad de las
levaduras. El empleo de WUAX al 4 % en la preparación de pan frito chino (youtiao), permitió obtener un producto de bajo contenido en grasa
y mejor valor nutrimental, al incrementar la humedad y la firmeza del producto,
así como disminuir el volumen específico y el contenido total
de aceite (37 %)
(Li y col.,
2017).
Por otra
parte, Marconi y col. (2000), sustituyeron en
un 50 % la sémola de trigo duro por fibra rica en AX de cebada, para
elaborar spaghetti. Aunque el spaghetti rico
en AX fue más oscuro que el spaghetti de trigo duro, presentó buenas
características de cocción respecto a la adhesividad, la firmeza y la materia
total liberada en el agua de lavado. Por
otro lado, Dexter y col. (2005), al sustituir el 20 % de sémola de trigo duro,
por harina de cebada sin cáscara (alto contenido de AX y β-glucanos),
observaron que el color del spaghetti era aceptable y la firmeza similar al spaghetti preparado con
100 % de sémola. En esta misma línea, Izydorczyk y col. (2005), encontraron que
el spaghetti enriquecido con fibra rica en AX, ofrece al consumidor un
menor tiempo de cocción, aceptable calidad
de cocción y un aumento y
diversificación del
valor nutrimental.
Recientemente,
se describió que la adición de AX de salvado de trigo (2 %) a la masa para
preparar fideo chino, contribuyó a mejorar las características de cocción
(absorción de agua y tiempo de cocción), textura (dureza, adhesividad,
elasticidad, cohesividad, gomosidad y masticabilidad), fuerza al quiebre,
flexibilidad y valor nutrimental de los fideos cocinados (Fan y col., 2016).
Actualmente, el interés de incorporar los AX y los AXOS, a los alimentos a base
de harina, va más allá de mejorar únicamente las características del producto:
se busca obtener un producto capaz de otorgar
un beneficio a
la salud.
AX y
AXOS como prebióticos
La tendencia actual de consumo responde cada vez más, a
la demanda de productos denominados “sanos” o “naturales”, con el fin de disminuir
el riesgo de padecer enfermedades crónico-degenerativas. Entre los productos
que satisfacen esta demanda se encuentran los alimentos enriquecidos con
prebióticos. Los prebióticos son ingredientes alimenticios no digeribles, que
tienen efectos benéficos en el hospedero, debido a la estimulación selectiva
del crecimiento o actividad de una o un número limitado de bacterias en el
colon, teniendo como consecuencia una mejora en la salud del huésped (Gibson
y Roberfroid, 1995).
Diversos
estudios in vitro
sobre AX y sus derivados, afirmaron que pueden ser fermentados por la
microbiota intestinal y estimular selectivamente el crecimiento y la actividad
de bacterias intestinales benéficas. Por ejemplo, Hopkins y col. (2003),
fermentaron AX y AX entrecruzados, extraídos
de endospermo de trigo en condiciones anaerobias y pH controlado. Los
medios de cultivo se inocularon con microbiota intestinal de niños. Estos autores
encontraron que la fermentación de AX y AX entrecruzados es lenta y se asocia
con un incremento en la formación de ácidos
grasos de cadena corta y un aumento significativo en la cuenta total de
anaerobios, en especial de Bacteroides
fragilis (Veillon y Zuber, 1898; Castellani y Chalmers, 1919). La fermentación lenta de los AX
también fue reportada por Kaur y col. (2011), quienes sometieron a los
AX, al igual que otras fibras, a una fermentación en suspensión fecal humana.
Las fermentaciones de los AX y β-glucanos
de cadena larga fueron lentas en una primera etapa, durante la cual se
produjeron concentraciones similares de ácidos grasos de cadena corta y bajos niveles de
gases.
La
estructura química de los AX puede influir en la fermentación y el crecimiento
selectivo o en la actividad de bacterias intestinales benéficas. Un claro
ejemplo de lo anterior es lo registrado por
Hughes y col. (2007), quienes fermentaron AX de trigo de diferente PM, utilizando heces fecales humanas. Si bien, todas las fracciones de AX mostraron
impacto bifidogénico comparables en la microflora, es de destacar que
los AX de menor PM (66 kDa) fueron
particularmente selectivos para Lactobacillus y Eubacterium. Entre tanto, la fermentación de todos los AX mostró un aumento en
la producción total de ácidos grasos de cadena corta, con una proporción
especialmente alta de ácido butírico.
La selectividad de Bifidobacterium y Lactobacillus por AX incrementó
cuando el PM
de los AX
disminuyó.
Por otra
parte, Reis y col. (2014), fermentaron AX de diferente estructura (GP y GS) en
medios con microbiota de adultos sanos. En ambos fermentados, se evidenció la
estimulación de la población bacteriana
benéfica (en especial Bifidobacterium)
y la producción de ácido grasos de cadena corta.
Sin embargo, los AX con mayor GP y menor GS presentaron la mayor proliferación de bacterias benéficas,
pero con una menor producción de ácidos grasos de cadena corta. De igual manera,
Ding y col. (2015), al estudiar la fermentación de AX de Psyllium
y de mucilago de linaza en
medios con microbiota de cerdo, observaron que los perfiles de ácidos
grasos de cadenas cortas fueron diferentes durante y al término del estudio.
En otro estudio, donde se fermentaron WUAX de trigo en un
sistema de cultivo mixto, se documentó un mayor índice
prebiótico de estos polisacáridos,
cuando fueron tratados previamente con enzimas endo-β-D-xilanasas
y feruloil esterasas (Vardakou y col., 2008).
Lo anterior puede estar relacionado con la complejidad estructural de
los WUAX, siendo necesario que la microbiota exprese una mayor cantidad de
enzimas para poder degradarlos. Igualmente,
la fermentación de WEAX en medios con contenido cecal de pollos de engorda, mostró
que la aplicación de enzimas hidrolíticas induce una mayor producción de
acetato y butirato
(Yacoubi y col.,
2016).
Los resultados in vitro antes
descritos han sido corroborados por estudios in vivo. Lopez
y col. (1999), alimentaron ratas con pan de un alto contenido en WEAX y
encontraron que los niveles de ácidos grasos de cadena
corta en el ciego (primera porción del intestino grueso) se incrementaron, en
especial el ácido propiónico. Un resultado similar reportaron Van-den-Abbeele y
col. (2011), quienes inocularon ratones con microbiota fecal humana y observaron
el efecto de la ingesta de AX de cadena larga. En dicho estudio, la microbiota
de los ratones, fue enriquecida con microorganismos de los filos Verrucomicrobia (Hedlund y col.,
1997), Firmicutes (Gibbons y Murray, 1978) y Bacteroidetes (Krieg y col.,
2010), además de contener diferentes especies de Bifidibacterium como B. bifidum (Tissier, 1900; Orla-Jensen, 1924), B. adolecentis y B. longum (Reuter, 1963). Los resultados demostraron que el suministro
de AX de cadena larga estimuló principalmente
el crecimiento de B. longum e incrementó los niveles de ácidos grasos de cadena
corta, induciendo principalmente la producción de propionato. El propionato puede ser absorbido por el
intestino, entrar al torrente sanguíneo y llegar al hígado por la vena porta,
donde se le ha asociado con la reducción de la síntesis del colesterol y mejora
de la sensibilidad a la insulina (Vanden-Abbeele y col.,
2011).
Por su
parte, Neyrinck y col. (2011), evaluaron en
ratones la habilidad de los WEAX (10 % p/p) para modular la microbiota
del intestino
y el metabolismo de lípidos después de
una dieta con alto contenido de grasa. El tratamiento con WEAX restauró el
número de bacterias que habían
disminuido a causa de la dieta, entre ellas Bacteroides (Castellani y Chalmers, 1919), Prevotella (Shah y Collins,
1990) y Roseburia (Stanton
y Savage, 1983). Además, el tratamiento con WEAX incrementó fuertemente el
contenido de bifidobacterias cecales, en particular Bifidobacterium animalis lactis (Meile
y col., 1997). Estos autores sugirieron que los WEAX empleados pueden
promover un impacto positivo en la salud a través de la modulación de la
microbiota intestinal.
Al igual
que las investigaciones sobre los AX, la fermentación de AXOS y su relación con la producción de ácidos grasos de cadena corta y estimulación selectiva, han demostrado el potencial de dichos oligosacáridos como
prebióticos. Los estudios in vitro se
han efectuado en simuladores del ecosistema microbiano del intestino humano
(SHIME, por sus siglas en inglés: Simulator
of the Human Intestinal Microbial Ecosystem), que se componen de
recipientes que simulan el estómago y el
duodeno, el yeyuno y el íleon, el colon ascendente, el colon transverso y el
colon descendente (Grootaert y col., 2009; Sanchez y col., 2009; ProDigest, 2016). Los análisis in vivo se han realizado tanto en ratas como en humanos (Grasten y
col., 2003; Cloetens y col., 2008; Van-Craeyveld y
col., 2008).
Grootaert
y col. (2009), analizaron el potencial
prebiótico de los AXOS en el SHIME. Durante el suplemento con AXOS,
encontraron un incremento en los niveles de lactato y propionato en el colon ascendente y transverso, respectivamente.
Si bien, el suplemento de los AXOS no
presentó efectos significativos en la composición de la microbiota, sí afectó
primordialmente el metabolismo microbiano, al “encender” la degradación
enzimática de los AXOS (arabinofuranosidasas, endo-β-D-xilanasas
y β-D-xilosidasas). De acuerdo con los
anteriores resultados, los autores
concluyeron que los AXOS tiene un alto potencial para desplazar parte de
la fermentación hacia las
partes distales del
colon.
Por su
parte, Sanchez y col. (2009), utilizaron el SHIME para evaluar el impacto del
GP y del GS de los AXOS (3-0.09; 3-0.25; 8-0.23; 15-0.26; 29-0.30), en el
balance de la fermentación de proteínas y carbohidratos, así como la composición
de la microbiota en el intestino grueso, y encontraron que en los experimentos de fermentación, los AXOS con bajo GP
(3 y 8) fueron primordialmente fermentados en el colon proximal; en cambio,
parte de los AXOS con alto GP (15 y 29) alcanzaron el colon distal. La
suplementación prolongada de AXOS con alto GP disminuyó los niveles de fenol y p-cresol, los cuales
son derivados de la fermentación microbiana de proteínas. Estos compuestos se asocian al riesgo
de alteraciones en el colon. Conjuntamente,
se incrementó la concentración de ácidos grasos de cadena corta en todos los
compartimentos representativos del colon. Además, aumentó significativamente la
cantidad de microorganismos promotores de buena salud como Lactobacillus, así como Bacteroides-Prevotella y Clostridium coccoides (Kaneuchi y col., 1976)-Eubacterium rectale (Prévot, 1938), por lo que concluyeron que, la suplementación de los AXOS
podría influir en la microbiota, para modular una respuesta positiva en la salud del hospedero.
Por otro
lado, Grasten y col. (2003), estudiaron en
humanos el efecto de la ingesta de pan enriquecido con AXOS y su
relación con la actividad metabólica de la microbiota fecal. Debido al consumo de pan enriquecido con AXOS, los sujetos de
estudio presentaron un aumento en los niveles de ácidos grasos de cadena corta
en heces, en donde el butirato mantuvo una
mayor proporción molar con respecto a acetato y propionato. Los niveles
de ácidos grasos en heces solo reflejan un parte de la producción de estos
ácidos, porque se absorben rápidamente en el colon ascendente. Sin embargo, una
alta concentración de ácidos grasos de cadena corta en heces, especialmente butirato, indica que la concentración de estos
ácidos en el colon descendente, el sitio de mayor incidencia de tumores,
también fue alta (Topping y Clifton, 2001).
El butirato se relaciona con la mejora de la función de la barrera de la mucosa
e induce la apoptosis de células tumorales a diferencia de acetato y propionato. Empero, acetato y propionato estimulan la biosíntesis de colesterol
(Fernández y col.,
2016).
Por su parte, Cloetens y col. (2008), caracterizaron la influencia
de los AXOS en la movilidad gastrointestinal y el metabolismo bacteriano en
humanos sanos. Para ello, suministraron a voluntarios una dieta cuyo contenido
de AXOS aumentó gradualmente. Al final del
periodo, el aumento de la cantidad de AXOS en la dieta no influyó en el
vaciado gástrico y el tiempo de tránsito intestinal, pero sí en la estimulación
del crecimiento bacteriano y
la actividad metabólica.
En
animales, específicamente en ratas, la administración de una dieta a base de
pan rico en AXOS, con diferentes grados de polimerización y sustitución, mostró
que los AXOS con bajo GP promovieron un incremento en la producción de acetato
y butirato en el colon y un aumento rápido en la concentración de la población
bacteriana de Bifidobacterium
en el ciego. Sin embargo, no se disminuyó la
concentración de ácidos grasos de cadena corta ramificados, los cuales
son considerados como marcadores de la
degradación de proteínas realizada
por la microbiota intestinal. En contraste, la suministración de AXOS con alto GP suprimió la concentración de ácidos grasos de cadena corta ramificados, por
lo que se evitó la degradación de proteínas, pero no aumentó la
concentración de butirato ni estimuló el
desarrollo del grupo Bifidobacterium. A su vez, la
ingestión de AXOS con GP
similar pero diferente GS, afectó de igual forma las características
intestinales, sugiriendo que la influencia se debe principalmente
al GP y
no al GS.
Los AXOS
con GP de 5 y GS de 0.27 presentaron los mejores efectos benéficos en el
intestino. Al comparase los efectos de estos AXOS
con respecto a la administración de inulina y fructo-oligosacáridos, se
obtuvieron efectos bifidogénicos similares y una mayor producción de butirato
(Van-Craeyveld y col., 2008), cuyo efecto
anti-tumoral se mencionó anteriormente. Esto permite colocar a los AXOS como compuestos que benefician a la salud tanto como los prebióticos inulina y fructo-oligosacáridos.
Otros
efectos benéficos de los AX y los AXOS en
la salud
Antiobesogénico
De
acuerdo a Neyrinck y col. (2011), la incorporación de AX, en la dieta de ratas
que consumían alimentos altos en grasa, disminuyó en los animales los problemas
relacionados a cambios en la microflora intestinal
y la obesidad (la
acumulación de colesterol hepático, reducción del tamaño de
adipocitos y peso corporal). Estos resultados fueron similares al cambiar el suministro de AX por AXOS (Neyrinck y col., 2012), por lo que concluyeron que tanto AX como sus derivados (AXOS) presetan propiedades relacionadas a la prevención de la obesidad y los desórdenes derivados
de dicho padecimiento.
Harding y col. (2014), documentaron en háms-ter, que el consumo de salvado de trigo (rico en AX) como
parte de una dieta inductora de obesidad e hipercolesterolemia,
disminuyó la masa grasa (7 %) y aumentó la masa magra corporal (8 %). Sin embargo, no encontraron diferencias respecto a
los niveles de colesterol plasmático
y de triglicéridos. Caso contrario, Tong y
col. (2014), observaron en hámsters hipercolesterolemicos, que el consumo de una dieta con AX de salvado de trigo disminuyó el colesterol total del plasma y el
colesterol-LDL al promover la excreción de lípidos en heces, vía de la
regulación de la
actividad
de la 3-hidroxi-3-metil-glutaril-CoA reductasa
(HMGCR) y colesterol 7-a-mono-oxigenasa
(CYP7A1). La síntesis y excreción de colesterol
en el hígado está regulada por la HMGCR
y CYP7A1, respectivamente (Sato y col.,
2003).
Así
mismo, Adam y col. (2001), observaron en ratones,
que una ingesta rica en AX puede modificar el metabolismo de lípidos, ya
que dicha dieta estimuló la disminución del colesterol plasmático y
triglicéridos en un 27 % y 40 %,
respectivamente. Estos resultados son similares
a los registrados por Lopez y col. (1999), quienes describieron que una dieta semipura
de WEAX permitió la disminución del 20 % y 25 % en el nivel del colesterol
plasmático y de triglicéridos, respectivamente, así como la disminución de la
acumulación de colesterol en el hígado de ratas. Sarma y col. (2018),
demostraron en ratones albinos, el beneficio que tiene la ingesta de AX de
mijo, durante una dieta con alto contenido de grasa. En dicho trabajo, la
suplementación de 0.5 g AX/kg en peso y 1.0 g AX/kg en peso por 10 semanas,
promovió la disminución del peso corporal y ganancia en peso, aunado a la reducción del perfil de lípidos en el suero,
la disminución de la inflamación y acumulación
de lípidos en el hígado y la modulación benéfica de la expresión de
genes del tejido hepático y adiposo blanco. Sin embargo, en humanos sanos con
sobrepeso y obesidad, la suplementación de AX durante 6 semanas, no
mostró efectos significativos en las concentraciones colesterol total,
colesterol LDL, colesterol HDL y triglicéridos (Salden y col., 2018). Los autores
explicaron estos resultados, en el hecho de
que los participantes tenían valores normales desde el comienzo del
estudio. Además, no se controló la dieta y actividad física de los
participantes, por lo que estos factores serían considerados en investigaciones futuras.
Regulador
de la glucosa
Hartvigsen
y col. (2013), reportaron que en ratas propensas a desarrollar diabetes tipo 2,
la ingesta de pan suplementado con WEAX derivó en una disminución de los
niveles de glucosa en ayunas y de insulina
plasmática. Además, se observó en el tejido adiposo sobrerregulación en la expresión de genes involucrados
en la cascada de señalización de insulina
y metabolismo de
glucosa y lípidos.
Por lo anterior, los autores
concluyeron que el consumo de pan de trigo suplementado con WEAX retarda
el desarrollo de diabetes tipo 2 en ratas. En este tipo de roedores, también se estudió la influencia del consumo de WUAX
y WUAX etrecruzados (rehidratados o no), en el
nivel de glucosa postprandial en sangre (Vogel y col., 2012). Estos autores observaron que a diferencia
de WUAX, los WUAX entrecruzados disminuyeron
significativamente el nivel de glucosa en sangre. La posible explicación
para dicho efecto la describen a partir de la
alta viscosidad en el bolo alimenticio, lo que probablemente disminuyó la
difusión de la glucosa hacia la superficie de absorción. Además, Sarma y
col. (2018) observaron en ratones, que la
inclusión de AX en una dieta alta en grasa, promovió la tolerancia a la glucosa, así como la disminución de las altas
concentraciones de lipopolisacáridos, de insulina y de leptina en el suero.
Altos niveles de estos compuestos es indicativo de una resistencia a la
insulina inducida por la endotoxemia metabólica que puede conducir a la diabetes
tipo 2 (Singh
y col., 2015).
Por su
parte, Christensen y col. (2013), trabajaron con cerdos la relación entre el
consumo de pan enriquecido con WEAX y la
respuesta inmediata de glucosa e insulina en
sangre. Los resultados mostraron que
ambas respuestas disminuyeron. La disminución inmediata de glucosa se justificó en similitud a lo
descrito anteriormente, mientras que la reducción de la secreción de insulina como consecuencia del bajo nivel
del flujo de glucosa.
En humanos, se ha registrado el efecto positivo
del consumo de AX (Sandberg y col., 2017) o AXOS (Boll y col., 2016) sobre la
tolerancia a la glucosa. De hecho, la Autoridad Europea de Seguridad
Alimentaria (Europen Food Safety Authority)
ha reconocido los efectos benéficos de los AX sobre la respuesta a la
glucosa post-prandial,
y la Unión Europea ha autorizado la
declaratoria de que “al consumo de AX, como parte de una comida, se le
atribuye la reducción del aumento de glucosa
en sangre después de esa comida” (Kellow
y Walker, 2018). Para ello, se revisaron 18 ensayos de investigación, de
los cuales, cuatro fueron en adultos sanos, tres en personas con trastornos metabólicos y uno en personas
con diabetes tipo
2.
Antioxidante
La
capacidad antioxidante de los AX y AXOS está
relacionada con el contenido de ácido ferúlico presente (Van-den-Ende y
col., 2011).
Por ejemplo, Malunga y Beta (2015), observaron que la capacidad
antioxidante de distintas fracciones de WEAX de trigo (aleurona y salvado rojo
y blanco) está asociada al
contenido
de ácido ferúlico y fenoles totales, donde el ácido ferúlico representa del 85
% al 95 %. En tanto, Ayala-Soto y col. (2014), analizaron la relación entre la
composición de azúcares, el perfil de ácidos hidroxicinámicos, fenoles totales
y la capacidad antioxidante de AX de diferentes fibras de maíz. Estos autores
encontraron que la capacidad antioxidante de los AX está relacionada principalmente
a la concentración de trímeros de ácido
ferúlico, seguido de ácido cumárico y fenoles totales.
La
capacidad antioxidante también puede estar influida por la complejidad
estructural de la molécula y la asociación
que tiene con otros componentes. Yadav y col. (2017), estudiaron la capacidad
antioxidante de diferentes materiales vegetativos compuestos de AX y celulosa.
Los valores más altos se detectaron en salvado de maíz y trigo, los cuales presentaron
la mayor proporción de AX: los autores
asociaron estos resultados a la estructura altamente ramificada de sus
componentes. Por su parte, Adam y col. (2002), de-
mostraron
en ratas, que después de la administración de una dieta a base de cereal (rica en
AX), se excretó en la orina un 95 % menos
de ácido ferúlico que el registrado después de
una dieta enriquecida con ácido ferúlico. Por ello, concluyeron que el efecto
antioxidante de los AX ferulados presentes en las harinas o cereales que se
ingieren está limitado por la baja biodisponibilidad del ácido ferúlico en el
organismo, como consecuencia del entrecruzamiento existente con otras
hemicelulosas y ligninas.
Asimismo,
Nordlund y col. (2012), cuantificaron la formación de metabolitos fenólicos
producidos por fermentación microbiana de salvado y aleurona (alto contenido de
AX), en condiciones que simulan el colon, observando que la formación del
metabolito ácido fenilpropiónico hidroxilado
dependió del contenido de ácido ferúlico, del tamaño de partícula y de la proporción de AX insolubles
presentes en las muestras. Malunga y col. (2017),
estudiaron el efecto protector de los WEAX
(diferente tipos y concentraciones) sobre la hidroperoxidación de
lípidos bajo condiciones gástricas simuladas, encontrando que, la formación de
los hidroperóxidos de lípidos permanecía ligeramente menor hasta una reducción del 30 %, dependiendo del tipo y
concentración de WEAX
en el ensayo.
Respecto al efecto antioxidante de AXOS, Veenashri
y Muralikrishna (2011), analizaron el perfil de ácidos fenólicos y la capacidad
antioxidante de AXOS derivados de diferentes cereales,
encontrando que el poder reductor depende principalmente de la concentración de
ácido ferúlico y su relación sinérgica y
aditiva con
otros compuestos fenólicos. En un estudio in
vivo, Maki y col. (2012), midieron la concentración de ácido
ferúlico presente en plasma sanguíneo de adultos mayores de 50 años, después de
ingerir cereal enriquecido con AXOS. Se relacionó el incremento de AXOS en el cereal ingerido, con un aumento en la
concentración de ácido ferúlico
plasmático. Sin embargo, la medición antioxidante del plasma no fue
significativamente superior al testigo. Los
autores explicaron dicho resultado en función de los bajos niveles de ácido ferúlico, comparado con otros compuestos antioxidantes presentes en el plasma, como ácido úrico, ácido ascórbico y
a-tocoferol.
En contraste, Ou y col. (2007), mediante pruebas en ratas con diabetes inducida,
confirmaron la alta capacidad antioxidante de
los AXOS, al observar que los AXOS pueden
reducir la peroxidación de lípidos en suero,
hígado y testículos. Este resultado concuerda con los ensayos in vitro realizados por Katapodis y col. (2003), quienes observaron
que los AXOS inhiben fuertemente la oxidación de la lipoproteína humana de baja
densidad.
Posiblemente, la diferencia en la actividad antioxidante entre los AX y los AXOS podría explicarse en términos del GP y GS de sus estructuras,
así como del entrecruzamiento de las
cadenas, ya que una mayor complejidad en la estructura no permitiría la
exposición del ácido ferúlico a
los compuestos oxidantes.
Anticancerígeno
Los
estudios in vivo
han situado a los AX y los AXOS como posibles agentes anti-cancerígenos. Entre ellos se encuentran los datos obtenidos
por Cao y col. (2011), quienes observaron que la administración oral de AX, a ratones
inducidos con tumores tipo S180, inhibió significativamente el crecimiento de
dichos tumores. Por su parte, Femia y col.
(2010), elaboraron un ensayo en cual
alimentaron ratas con una dieta rica en AXOS y las trataron con un
agente carcinogénico, inductor de dos tipos de lesiones en el colon. El consumo
de este oligosacárido, por un periodo de 30
d, causó la reducción significativa de dichas lesiones, corroborando que la ingesta de AXOS puede tener un efecto benéfico en la disminución de
riesgo de cáncer.
La fermentación
de proteínas no es un proceso benéfico en el colon, ya que se producen
compuestos como el p-cresol,
fenol y amonio que se consideran promotores
de cáncer. El consumo de AX y AXOS promovió la protección intestinal de cerdos alimentados con una
dieta rica en proteína (Belobrajdic y col.,
2012; Zhang y col., 2015; Williams y col.,
2016), al disminuir la concentración de dichas sustancias en
heces.
Sugawara y col. (1990), encontraron que la suplementación
de extracto de pericarpio de maíz, a voluntarios
sanos, promovió la disminución de la actividad de la enzima β‑glucuronidasa y del contenido de amonio en heces. Muchos
compuestos se conjugan con el ácido glucurónico en el hígado y son excretados vía bilis al tracto
gastrointestinal (Rowland y Mallet, 1986). En estado glucuronidado, estos compuestos son
inactivos, se absorben poco en el intestino y se excretan en las heces. Sin embargo, la enzima β-glucuronidasa
presente en el intestino, remueve la fracción
glucurónida de estos conjugados
produciendo metabolitos que pueden ser reabsorbidos en el intestino. Estos metabolitos son altamente tóxicos y se consideran promotores de cáncer, por lo
que la actividad de β-glucuronidasa se considera
como un biomarcador de riesgo de cáncer
(Wallace y col., 2015). El amonio al ser
considerado un carcinógeno potencial,
se desea que se excrete por vía fecal en vez de la vía urinaria, lo que
significaría que la absorción del tóxico se realizó a través de la mucosa del
colon (Broekaert y col., 2011). Este cambio en la vía de excreción de
amonio fue observado por Cloetens y col.
(2008), quienes suministraron a
voluntarios sanos, pan enriquecido con
AXOS. Para estudiar la influencia de los AXOS en el metabolismo de amonio se utilizó ureido-[15N, 15N’]-lactosa;
dicho biomarcador es convertido a amonio-15N en el colon. El consumo
de AXOS redujo significativamente la secreción urinaria de amonio-15N con un correspondiente incremento de amonio-15N
en las heces. Este cambio se explicó
considerando que los AXOS estimulan la
fermentación bacteriana de carbohidratos en el colon, aumentado así la ingesta
y la asimilación del
nitrógeno en estas
bacterias.
Además,
en otro estudio donde se suministró a humanos sanos pan enriquecido con AXOS,
se observó que disminuyó la producción de ácidos orgánicos asociados a la
fermentación de proteínas, como el isobutirato, isovalerato, valerato y caproato (Walton y col., 2012). También
se ha demostrado que la estructura de los AX
y AXOS influye en la fermentación de proteínas.
Damen y col. (2011), hicieron un
estudio donde alimentaron a ratas con dietas que incluía WEAX, WUAX y AXOS en
forma individual o combinada. En
general, los niveles de
isobutirato e isovalerato disminuyeron tanto
en el ciego como en colon en aquellas ratas que consumieron dieta con WEAX, AXOS,
WEAX+AXOS y WUAX+WEAX+AXOS. La reducción
más fuerte se observó en ratas que consumieron dieta con WEAX, mientras que en
las que consumieron dietas con WUAX y WUAX+AXOS
no se presentó
efecto positivo.
Inmunomodulador
Samuelsen
y col. (2011), realizaron ensayos in
vitro para determinar la actividad biológica de los AX sobre la habilidad de modular la
actividad de NF-kB en monocitos, así como
la proliferación de dos líneas celulares
del epitelio intestinal (células Caco-2 y HT-29) y sus respectivas
secreciones de citosinas tipo IL-8 (interleucina 8). Los resultados mostraron
que los AX no presentaron efecto significativo en la proliferación y la
secreción de IL-8 de dichas líneas celulares, ni tampoco en la actividad de NF-kB, por lo que no
encontraron actividad inmunomodulatoria de los AX.
En otro
estudio, se evaluó el efecto inmunomodulador de los AX sobre macrófagos humanos en una línea celular de monocitos (U937), midiendo
los niveles de óxido nítrico (Zhang y col., 2016). El óxido nítrico es un
mediador en la inflamación y defensas del hospedero mediante diferentes mecanismos de acción. Como resultado, las células U937, tratadas con AX, incrementaron la producción de óxido
nítrico con respecto al control: los valores de producción dependieron de la
concentración y PM de los AX utilizados. Por
lo que se sugirió que los AX pueden
aumentar la respuesta innata inmune en ausencia de infección o
enfermedad.
Los
estudios in vivo han
mostrado resultados alentadores respecto a
la influencia de los AX en el sistema inmune. Por ejemplo, tanto en ratones
sanos, como en ratones infectados con
células tumorales, se demostró que la administración intragástrica de WEAX, de
cáscara de maíz, induce la reducción de alergias y aumenta la producción de interferóngama y citocinas tipo IL-2, así
como la activación de células NK
(Natural Killer) (Ogawa y col., 2005). En semejanza con lo anterior, la
administración oral de AX a ratones con tumores tipo S180 estimuló la
actividad fagocítica de macrófagos y de
células NK, la producción de
citocinas tipo IL-2 y la proliferación de linfocitos (Cao y col., 2011).
En un modelo murino con inducción de tumores
NB1691, la terapia con células NK estimuladas con AX (incubación en
medio que incluía AX de salvado de arroz), provocó el incremento de la actividad de las células NK e inhibió el progreso de dichos tumores (Pérez-Martínez y
col., 2015).
Además,
Zhou y col. (2010), demostraron que la actividad inmunoreguladora de AX varía
de acuerdo a su estructura. Para lograrlo, administraron oralmente diferentes
AX a ratones albinos (BALB/c). El primer AX
(AX1) no contenía ácido ferúlico, su contenido de proteína fue de 4 %,
con un PM de 351 kDa y un GS de 0.83, mientras que el segundo (AX2), contenía
43 mg ácido ferúlico/100 g AX, un 9 % de
proteína, un PM de 32 kDa y un GS de 0.56. Estos autores reportaron que
el consumo de ambos polisacáridos ejerció una
potente
estimulación en la respuesta inmune, mejorando
la proliferación de linfocitos. Sin embargo, la mayor fagocitosis de
macrófagos se registró
en ratones tratados
con AX2.
También se reportó que la estructura de AXOS influye en la respuesta del sistema inmune de aves de corral inoculadas oralmente con Salmonella
enteritidis (Gartner, 1888; Castellani y Chalmers,
1919). Dichas aves se alimentaron con AXOS de distinto GP durante 37 d. Durante
los primeros 11 d, después de la inoculación,
se observó que todas las aves tratadas con AXOS inhibieron la colonización
de S. enteritidis en el bazo, aunque el mayor porcentaje de inhibición se
dio en AX con alto
GP (Eeckhaut y
col., 2008).
Broekaert y col. (2011), sugirieron que el efecto
de los prebióticos en la modulación de la microbiota
intestinal no es prueba por sí misma de los efectos benéficos, excepto
cuando dicha modulación involucra la
disminución de bacterias patógenas y
sus efectos dañinos. Sin embargo,
esta sugerencia no considera que los
prebióticos puedan actuar estimulando selectivamente
la actividad de algunos organismos produciendo sustancias benéficas que
impactan los procesos del cuerpo, como son
el tránsito intestinal, las funciones
inmunitarias, el metabolismo de lípidos, el metabolismo energético y la
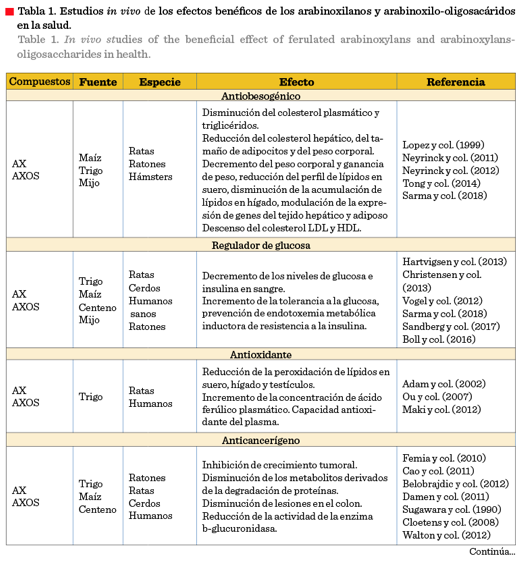
inhibición del desarrollo de tumores, entre otros. En ese sentido, los
resultados obtenidos, en los estudios sobre la ingesta de los AX y los AXOS, han
puesto de manifiesto la congruencia de ser considerados como promotores de la
buena salud, ya que se les ha asociado como posibles agentes reductores de
colesterol (Adam y col., 2001), antioxidantes (Ou y col., 2007), antitumorales
y benefactores del sistema inmune (Cao y
col., 2011) (Tabla
1).

CONCLUSIONES
Los
arabinoxilanos y arabinoxilo-oligosacáridos han demostrado estimular el
crecimiento y actividad de bacterias benéficas, así como generar respuestas
biológicas asociadas a la buena salud del hospedero, por su efecto antiobesogénico, regulador de la glucosa, antioxidante,
anticancerígeno e inmunomodulador. Los AX y los AXOS al ser obtenidos de subproductos
del procesamiento de los granos de cereales, aportarían
un efecto benéfico adicional a la dieta. Es importante destacar que los
AX y los AXOS pueden contener en su estructura ácido ferúlico, lo cual les
proporciona actividad antioxidante, siendo hasta donde la literatura reporta,
el único prebiótico con esta propiedad. Se requiere investigación adicional enfocada a estudiar la relación entre la estructura
química de los AX y los AXOS (grado de sustitución, contenido de ácido ferúlico,
peso molecular, distribución de arabinosa y ácido ferúlico en la cadena de
xilosa) y el efecto prebiótico y promotor de la buena salud de estos
compuestos. Es posible que en un futuro cercano, la generación de nuevo
conocimiento sobre los AX y los AXOS siente las bases para su aplicación como
prebiótico en la industria alimentaria, biomédica o farmacéutica, entre otras, lo cual permitiría además dar valor
agregado a los cereales o subproductos de cereales, de los cuales pueden
ser extraídos estos
componentes.
REFERENCIAS
Adam, A. V.,
Crespy, V., Levrat-Verny, M. A., Leenhardt, F., Leuillet, M., Demigne, C., and
Remesy, C. (2002). The bioavailability of ferulic acid is governed primarily by
the food matrix rather than its metabolism in intestine and liver in rats. Journal of
Nutrition. 132(7): 1962-1968.
Adam, A. V., Levrat-Verny, M. A., Lopez, H. W., Leuillet, M., Demigne, C.,
and Remesy, C. (2001). Whole wheat and triticale flours with differing
viscosities stimulate cecal fermentations and lower plasma and hepatic lipids in rats. Journal of Nutrition. 131(6):
1770-1776.
Asp, N. G.,
Björck, I., and Nyman, M. (1993). Physiological
effects of cereal dietary fibre. Carbohydrate
Polymers. 21(2-3): 183-187.
Ayala-Soto, F. E.,
Serna-Saldívar, S. O., García-Lara, S., and Pérez-Carrillo, E. (2014).
Hydroxy-cinnamic acids, sugar composition and antioxidant capacity of arabinoxylans extracted from different maize fiber
sources. Food
hydrocolloids. 35: 471-475.
Ayala-Soto, F. E.,
Serna-Saldívar, S. O., and Welti-Chanes, J. (2017). Effect of arabinoxylans and
laccase on batter rheology and quality of yeast-leavened gluten-free
breads. Journal of Cereal Science. 73: 10-17.
Belobrajdic, D.
P., Bird, A. R., Conlon, A. M., Williams, B. A., Kang, S., McSweeney, C. S., …, and Topping, D. L. (2012). An arabinoxylan-rich
fraction from wheat enhances caecal fermentation and protects colonocytes DNA
against diet-induced damage in pigs. British Journal of
Nutrition. 107(9): 1274-1282.
Birkett, A. and
Cho, S. (2013). Cereal fiber and health:
current knowledge. Cereal Food World. 58(6): 309-313.
Boll, E. V. J.,
Ekström, L. M. N. K., Courtin, C. M., Delcour, J. A., Nilsson, A. C., Björck,
I. M. E., and Östman, E. M. (2016). Effects of wheat bran extract rich in
arabinoxylan oligosaccharides and resistant starch on overnight glucose
tolerance and markers of gut fermentation in
healthy young adults. European Journal of Nutrition. 55 (4): 1661–70.
Broekaert, W. F.,
Courtin, C. M., Verbeke, K., Van-de-Wiele, T., Verstraete, W., and Delcour, J.
A. (2011). Prebiotic and other
health-related effects of cereal-de-rived arabinoxylans, arabinoxylan-oligosaccharides, and
xylooligosa-ccharides. Critical Reviews in
Food Science and
Nutrition. 51(2): 178-194.
Cao, L., Liu, X.,
Qian, T., Sun, G., Guo, Y., Chang, F., Zhou, S., and Sun, X. (2011). Antitumor
and immuno-modulatory activity of
arabinoxylans: a major constituent of
wheat bran. International Journal of
Biological Macromolecules. 48(1): 160-164.
Castellani, A. and Chalmers, A. J. (1919). XXXVI: Bacteroideae. In
Manual of tropical medicine, third edition (pp. 959-960). New York, USA: Williams Wood & Co.
Christensen,
K. l., Hedemann, M. S., Lære, H. N., Jørgensen, H., Mutt, S. J., Herzig, K. H.,
and Bach-Knudsen, K. E. (2013). Concentrated arabinoxilan but not concentrated
b-glucan in wheat bread has similar effects
on postprandial insulin as whole-grain rye in porto-arterial
catheterized pigs. Journal of Agricultural and
Food Chemistry. 61(32): 7760-7768.
Cloetens, L., De-Preter, V., Swennen, K.,
Broekaert, W., Courtin, C. M., Delcour, J. A., …, and
Verbeke, K. (2008). Dose-response effect of
arabinoxylooligo-saccharides on gastrointestinal motility and on colonic
bacterial metabolism in healthy volunteers. Journal of the American College of
Nutrition.
21(4): 512-518.
Courtin, C. M. and Delcour, J. A. (2002).
Arabinoxylans and endoxylanases in wheat flour breadmaking. Journal of
Cereal Science. 35(3): 225-243.
Damen, B., Verspreet, J., Pollet, A.,
Broekaert, W. F., Delcour, J. A., and
Courtin, C. M. (2011). Prebiotics effects and
intestinal fermentation of cereal arabinoxylans and arabinoxylan
oligosaccharides in rats depend strongly on their structural properties and
joint presence. Molecular Nutrition & Food Research. 55(12): 1862-1874.
Dexter, J. E., Izydorczyk, M. S.,
Marchylo, B. A., and Schlichting, J. M. (2005). Texture and colour of pasta
containing mill fractions from hullless barley genotypes with variable content
of amylose and fibre. In. S. P. Cauvin, S.
S. Salmon, and L. S. Young (Eds.), Using Cereal Science and Technology for
the Benefit of Consumers (pp.
489-493). Boca Raton, USA: CRC Press.
Ding, H. H., Cui, S. W., Goff, H. D., and
Gong, J. (2015). Short-chain fatty acid profiles from flaxseed dietary fibres
after in
vitro fermentation
of pig colonic digesta: Structure–function
relationship. Bioactive Carbohydrates and
Dietary Fibre. 6(2): 62-68.
Döring, C., Grossmann, I., Roth, M.,
Jekle, M., Koehler, P., and Becker, T. (2017a). Effect of rye bran particles on
structure formation properties of rye dough and bread: bran particles and rye
dough structure. Journal
of Food Processing and Preservation. 41(4): e12998.
Döring, C., Hussein, M. A., Jekle, M., and
Becker, T. (2017b). On the assessments of arabinoxylan localization and enzymatic modifications for enhanced
protein networking and its structural impact on rye dough and
bread. Food
Chemistry. 229: 178–187.
Eeckhaut, V.,
Van-Immerseel, F., Dewulf, J., Pasmans, F., Haesebrouck, F., Ducatelle, R., …, and Broekaert, W. F. (2008). Arabinoxylooligosaccharides from wheat bran inhibit Salmonella colonization in broiler
chickens. Poultry Science. 87(11): 2329-2334.
Fan, L., Ma, S.,
Wang, X., and Zheng, X. (2016). Improvement of Chinese noodle quality by
supplementation with arabinoxylans from wheat
bran. International Journal of Food
Science & Technology. 51(3): 602–608.
FAO, Food and Agriculture Organization of the Nations (2017). Food and
Agriculture Organization of the United Nations
Statistics Division (FAOSTAT). [En línea]. Disponible en:
www.fao.org/faostat/es/#data/QC. Fecha de consulta: 2
de octubre de
2017.
Femia, A. P.,
Salvadori, M., Broekaert, W. F., Francois, I. E., Delcour, J. A., Courtin, C. M., and Caderni,
G. (2010). Arabinoxylan-oligosaccharides
(AXOS) reduce preneoplastic lesions in the colon of rats treated with 1,2-dimethylhydrazine
(DMH). European Journal of
Nutrition. 49(2): 127-132.
Fernández, J.,
Redondo-Blanco, S., Gutiérrez-del-Río, I.,
Miguélez, E. M., Villar, C. J., and Lombó, F. (2016). Colon microbiota
fermentation of dietary prebiotics towards short-chain fatty acids and their
roles as anti-inflammatory and antitumour
agents: A review. Journal of Functional
Foods. 25: 511-522.
Fincher, G. B. and Stone, B. A. (1974). A water-soluble arabinogalactan-peptide from
wheat endosperm. Australian Journal of
Biological Sciences. 27(2): 117-132.
Gartner, E. (1888): Über die fleischvergiftung
in Frankenhausen am Kyffhäuser und dererreger derselben. Korrespondenzblatt
des Allgemeinen Ärztlichen Vereins von Thüringen. 17: 573-600.
Gibbons, N. E. and
Murray, R. G. E. (1978). Proposals concerning the higher taxa of bacteria. International Journal of Systematic Bacteriology. 28(1): 1-6.
Gibson, G. R. and
Roberfroid, M. B. (1995). Dietary modulation of the human colonic microbiota:
Introducing the concept of prebiotics. Journal of
Nutrition. 125(6): 1401-1412.
Grasten, S.,
Liukkonen, K. H., Chrevatidis, A., El-Nezami, H., Poutanen, K., and Mykkänen,
H. (2003). Effects of wheat pentosan and inulin on the metabolic activity of
fecal microbiota and on bowel function in
healthyhumans. Nutrition Research. 23(11): 1503-1514.
Grootaert, C.,
Delcour, J. A., Courtin, C. M., Broekaert, W. F., Verstraete, W., and
Van-de-Wiele, T. (2007). Microbial metabolism and prebiotic potency of arabinoxylan
oligosaccharides in the human intestine. Trends in Food Science & Technology. 18(2): 64-71.
Grootaert, C.,
Van-den-Abbeele, P., Marzorati, M., Broekaert,
W. F., Courtin, C. M., Delcour, J. A., and Van-de-Wiele, T. (2009).
Comparison of prebiotic effects of arabinoxylan
oligosaccharides and inulin in a simulator of the human intestinal
microbial ecosystem. FEMS Microbiology Ecology. 69(2): 231-242.
Grossmann, I.,
Döring, C., Jekle, M., Becker, T., and
Koehler, P. (2016). Compositional Changes and Baking Performance of Rye
Dough As Affected by Microbial Transglutaminase
and Xylanase. Journal of Agricultural and
Food Chemistry. 64(28):
5751-5758.
Harding, S. V.,
Sapirstein, H. D., Rideout, T. C., Marinangeli, C. P. F., Dona, A. K. M., and
Jones, P. J. H. (2014). Comsuption of
wheat bran modified by autoclaving reduces fat mass in hamsters. European
Journal of Nutrition. 53(3): 793-802.
Hartvigsen, M. L.,
Jeppesen, P. B., Lærke, H. N., Njabe, E. N., Bach-Knudsen, K. E., and
Hermansen, K. (2013). Concentrated Arabinoxylan in wheat bread has beneficial
effects as rye breads on glucose and change in gene expressions in
isulin-sensitive tissues of zuckerdiabetic fatty (ZDF) rats. Journal of
Agricultural and Food
Chemistry. 61(21): 5054-5063.
Hedlund, B. P.,
Gosink, J. J., and Staley, J. T. (1997). Verrucomicrobia div. nov., a new division of the Bacteria containing three new species of Prosthecobacter. Antonie van Leeuwenhoek. 72(1): 29-38.
Hopkins, M. J.,
Englyst, H. N., Macfarlane, S., Furrie, E., Macfarlane, G. T., and McBain, A.
J. (2003). Degradation of cross-linked and non-crosslinked arabi-noxylans by
the intestinal microbiota in children. Applied and Environmental Microbiology. 69(11): 6354-6360.
Hughes,
S. A., Shewry, P. R., Li, L., Gibson, G. R., Sanz, M. L., and Rastall, R. A. (2007).
In vitro fermentation by human fecal microflora of wheat arabinoxylans. Journal of
Agricultural and Food Chemistry. 55(11): 4589-4594.
Izydorczyk, M. S.
and Biliaderis, C. G. (2007). Arabinoxylans: Technologically and nutritionally functional plant polysacharides. In C. G.
Biliaderis and M. S. Izydorczyk
(Eds.), Functional Food Carbohydrates (pp. 252-253).
Boca Raton, USA: CRC Press.
Izydorczyk, M. S.,
Lagassé, S. L., Hatcher, D. W., Dexter, J. E., and Rossnagel, B. G. (2005). The
enrichment of Asian noodles with fiber-rich fractions derived from roller milling of hull-less barley. Journal of the Science of Food
and Agriculture. 85(12):
2094-2104.
Jones, J. M.,
Peña, R., Korczak, R., and Braun, H. J. (2015).
CIMMYT series on carbohydrates, wheat, grains, and health: carbohydrates,
grains, and wheat in nutrition and health: an overview.
Part I. Role of carbohydrates
in health. Cereal Foods Wold. 60(5): 224-233.
Kaneuchi, C., Benno, Y., and Mitsuoka, T. (1976). Clostridium
coccoides, a new species from the feces of mice. International
Journal of Systematic Bacteriology. 26(4): 482-486.
Katapodis, P.,
Vardakou, M., Kalogeris, E., Kekos, D., Macris, B. J., and Christakopoulos, P.
(2003). Enzymic production of a feruloylated oligosaccha-ride with antioxidant activi-ty from wheat flour
arabinoxylan. European Journal of
Nutrition. 42(1): 55-60.
Kaur, A. R.,
Rumpagaporn, D. J., Patterson, P., and Hamaker, B. R. (2011). In vitro batch
fecal fermentation comparison of gas and short-chainfatty acid production using
“slowly fermentable” dietary fibers. Journal of Food
Science. 76(5): H137-H142.
Kellow, N. J. and
Walker, K. Z. (2018). Authorised EU health
claim for arabinoxylan. In M. J. Sadler (Ed.), Foods, Nutrients and Food Ingredients with
Authorised EU Health Claims (pp 201–218). Melbourne, Australia: Woodhead
Publishing.
Kirchengast,
S. (2014). Physical inactivity from the viewpoint
of evolutionary medicine. Sports. 2(2): 34-50.
Koegelenberg, D.
and Chimphango, A. F. A. (2017). Effects of
wheat-bran arabinoxylan as partial flour replacer on bread properties. Food Chemistry. 221: 1606–1613.
Krieg, N. R.,
Ludwig, W., Euzéby, J., and Whitman, W. B. (2010). Phylum XIV. Bacteroidetes
phyl. nov. In N. R. Krieg, J. T. Staley, D. R. Brown,
B. P. Hedlund, B. J. Paster, N. L. …, and
Parte, A. (Eds), Bergey’s Manual of Systematic Bacteriology (Second edition),
(pp. 25-469). New York,
USA: Springer.
Li, L., Wang, W.,
Zhou, S., Wang, L., Qian, H., Li, Y., …, and Qi, X.
(2017). Effects of water-unextractable arabinoxylans on the physicochemical and
rheological properties of traditional Chinese youtiao. International
Journal of Food
Science & Technology.
17: 1-7.
Lopez, H. W.,
Levrat, M. A., Guy, C., Messager, A., Demigné, C., and Rémésy, C. (1999).
Effects of soluble corn bran arabinoxylans on cecal digestion, lipid metabolism, and mineral balance (Ca, Mg) in rats. The Journal of Nutritional Biochemistry. 10(9): 500-509.
Lu, Z. X., Walker,
K. Z., Muir, J. G., Mascara, T., and O’Dea, K. (2000). Arabinoxylan fiber, a by
product of wheat flour processing, reduces the postprandial glucose response
in normoglycemic subjects. The American Journal of Clinical
Nutrition. 71(5): 1123-1128.
Maki, K. C.,
Gibson, G. R., Dickman, R. S., Kendall, C. W. C., Chen, O., Costabile, A., …,
and Zello, G. A. (2012). Digestive and
physiologic effects of a wheat bran extract, arabinoxylan-oligosaccharide, in
breakfast cereal. Nutrition. 28(11): 1115-1121.
Malunga, L. N. and
Beta, T. (2015). Antioxidant capacity of water-extractable arabinoxylan from commercial barley, wheat, and wheat fractions. Cereal
Chemistry. 92(1): 29-36.
Malunga, L. N.,
Izydorczyk, M., and Beta, T. (2017). Effect
of water-extractable arabinoxylans from wheat aleurone and bran on lipid
peroxidation and factors influencing their antioxidant capacity. Bioactive Carbohydrates and Dietary
Fibre. 10: 20-26.
Marconi,
E., Graziano, M., and Cubadda, R. (2000). Composition and utilization of barley pearling
by-products for making functional pastas rich in dietary fiber and β-glucans. Journal of Cereal Science. 77(2): 133-139.
Meile, L., Ludwig, W., Rueger, U., Gut, C., Kaufmann, P., Dasen, G., …, and Teuber, T. (1997). Bifidobacterium lactis sp. nov.,
a moderately oxygen tolerant species isolated from fermented milk. Sysematic
and Applied Microbiology. 20: 57-64.
Messia,
M. C., Reale, A., Maiuro, L., Candigliota, T., Sorrentino, E., and Marconi, E. (2016). Effects of
prefermented wheat bran on dough and bread characteristics. Journal of Cereal Science. 69: 138–144.
Neyrinck, A. M.,
Possemiers, S., Druart, C., Van-de-Wiele, T., De-Backer, F., Cani, P. D.,
Larondelle, Y., …, and Delzenne, N. M. (2011).
Prebiotic effects of wheat arabinoxylan
related to the increase in bifidobacteria, Roseburia and Bacteroides/Prevotella
in dietinduced obese mice. PLoSOne. 6(6): e20944.
Neyrinck, A. M.,
Van-Hée, V. F., Piront, N., De-Backer, F., Toussaint, O., Cani, P. D., and
Delzenne, N. M. (2012). Wheat-derived
arabinoxylan oligosaccharides with prebiotic effect increase satietogenic
gut peptides and reduce metabolic
endotoxemia in diet-induced obese mice. Nutrition
& Diabetes. 2(1): 1-9.
Nordlund, E.,
Aura, A. M., Mattila, I., Kössö, T., Rouau, X., and Poutanen, K. (2012).
Formation of phenolic microbial metabolites and short-chain fatty acids from
rye, wheat, and oat bran and their fractions in the metabolical in in vitro colon model. Journal of Agricultural and Food
Chemistry. 60(33): 8134-8145.
Ogawa, K.,
Takeuchi, M., and Nakamura, N. (2005).
Immunological effects of partially hydrolyzed arabinoxylan from corn husk in
mice. Bioscience, Biotechnology, and Biochemistry. 69(1): 19-25.
Orla-Jensen, S.
(1924). La classification des batteries lactiques. Le Lait.
4: 468-474.
Ou, S. Y.,
Jackson, G. M., Jiao, X., Chen, J., Wu, J. Z., and Huang, X. S. (2007).
Protection against oxidative stress in diabetic rats by wheat bran feruloyl
oligosaccharides. Journal of Agricultural and Food Chemistry. 55(8): 3191-3195.
Patel, S. and
Goyal, A. (2012). The current trends and future perspectives of prebiotics
research: A review. 3 Biotech. 2(2): 115-125.
Pérez-Martínez, A., Valentín, J., Fernández, L., Hernández-Jiménez, E.,
López-Collazo, E., Zerbes, P., …, and Díaz, M. Á. (2015). Arabinoxylan rice bran (MGN-3/Biobran) enhances natural killer cellmediated cytotoxicity against neuroblastoma
in Vitro and in Vivo. Cytotherapy. 17(5): 601–612.
Prévot, A. R. (1938).
Études de systématique bactérienne. III. Invalidité du genre Bacteroides
Catellani et Chalmers démembrement et reclassification. In G.
Masson (Ed.), Annales de l’lnstitut Pasteur. (pp. 285-307). Paris, Francia:
Institut Pasteur.
ProDigest, Laboratory of Microbiol Ecology and Technology, Ghent
University (2016). Shime and Shime, in Gastrointestinal
Expertise. ProDigest. [En línea]. Disponible en: www.prodigest.eu/en/technology/shime-and-mshime.
Fecha de consulta: 2
de octubre de 2017.
Reis, S. F.,
Gullon, B., Gullon, P., Ferreira, S., Maia, C. J., Alonso, J. L., …, and Abu-Ghannam, N. (2014). Evaluation of the prebiotic
potential of arabinoxylans frombrewer’s
spent grain. Applied Microbiology and Biotechnology. 98(22): 9365-9373.
Reuter, G. (1963).
Vergleichende untersuchunge uberdie Bifidus-flora im sauglings und
erwashenenstuhlz. Zentralblatt fur Bakteriologie, Parasitenkunde, Infektionskran-kheitenund Hygiene. Abteilung I.
191: 486-507.
Rowland, I. R. and
Mallet. A. K. (1986). Dietary fiber and the
gut microflora. Thier effects on toxicity in “new concepts and
development in toxicology.” In P. L. Chambers, P. Gehring, and F. Sakai (Eds.),
New concepts
and developments in toxicology (pp. 125–138). B. V. London: Elsevier Science Publiser.
Rouau, X.,
El-Hayek, M. L., and Moreau, D. (1994). Effect
of a enzyme preparation containing pentosanases
on the bread-making quality of flours in
relation to changes in pentosan properties. Journal of
Cereal Science. 19(3): 259-272.
Saeed, F., Arshad,
M. U., Pasha, I., Suleria, H. A. R., Arshad,
M. S., Qamar, A., …, and Sultan, S. (2015). Effect of arabinoxylan and
arabinogalactan on textural attributes of bread. Journal of
Fodd Processing and Preservation. 39(6): 1070-1088.
Salden, B. N.,
Troost, F. J., Wilms, E., Truchado, P., Vilchez-Vargas, R., Pieper, D. H., …,
and Masclee, A. A. (2018, en prensa). Reinforcement of intestinal epithelial
barrier by arabinoxylans in overweight and obese subjects: A randomized
controlled trial: Arabinoxylans in gut
barrier. Clinical Nutrition. DOI:
10.1016/j.clnu. 2017.01.024.
Samuelsen, A. B.,
Rieder, A., Grimmer, S., Michaelsen, T. E., and Knutsen, S. H. (2011).
Immunomodulatory activity of dietary fiber: arabinoxylan and mixed-linked Beta-glucan isolated from barley show
modest activities in vitro. International Journal
of Molecular Sciences. 12(1): 570-587.
Sandberg, J. C.,
Björck, I. M. E., and Nilsson, A. C. (2017). Effects of whole grain rye, with
and without resistant starch type 2 supplementation, on glucose tolerance, gut
hormones, inflammation and appetite regulation in an 11–14.5 hour perspective;
a randomized controlled study in healthy
subjects. Nutrition Journal. 16(1): 25.
Sarma, S. M.,
Singh, D. P., Singh, P., Khare, P., Mangal, P., Singh, S., …,
and Kondepudi, K. K. (2018). Finger millet arabinoxylan protects mice from
highfat diet induced lipid derangements, inflammation, endotoxemia and gut bacterial dysbiosis. International Journal of Biological
Macromolecules. 106: 994-1003.
Sanchez, J. I.,
Marzorati, M., Grootaert, C, M., Baran, M., Van-Craeyveld, V., Courtin, C. M.,
and Van-de-Wiele, T. (2009). Arabinoxylan-oligosaccharides (AXOS) affect the protein/carbohydrate fermentation
balance and microbial population dynamics of
the simulator of human intestinal
microbial ecosystem. Microbial Biotechnology. 2(1): 101-113.
Saulnier, L.,
Sado, P. E., Branlard, G., Charmet, G., and Guillon, F. (2007). Wheat
arabinoxylans: Exploiting variation in amount and composition to develop enhanced
varieties. Journal of Cereal
Science. 46(3): 261-281.
Sato, K., Ohuchi,
A., Sook, S. H., Toyomizu, M., and Akiba, Y.
(2003). Changes in mRNA expression of 3-hydroxy-3-methylglutaryl
coenzyme A reductase and cholesterol 7
alphahydroxylase in chickens. Biochimica
et Biophysica Acta (BBA) - Gene Structure
and Expression. 1630(2–3): 96-102.
Shah, H. N. and
Collins, D. M. (1990). Prevotella, a new genus to include Bacteroides melaninogenicus
and related species formerly classified in the genus Bacteroides. International Journal of Systematic
Bacteriology. 40(2): 205-208.
Singh, D. P.,
Khare, P., Zhu, J., Kondepudi, K. K., Singh, J., Baboota, R. K., …, and Bishnoi,
K. (2015). A novel cobiotic-based preventive approach against high-fat
diet-induced adiposity, nonalcoholic fatty liver and gut derangement in mice. International
Journal Of Obesity. 40: 487.
Smith, M. M. and
Hartley, R. D. (1983). Ocurrence and nature of ferulic acid substitution of
cellwall polysaccharides in graminaceous plants. Carbohydrate Research. 118: 65-80.
Stanton, B. and
Savage, D. C. (1983). Roseburia cecicola gen. nov., sp. nov., a motile,
obligately anaerobic bacterium from a mouse cecum. International
Journal of Systematic
Bacteriology. 33(3):
618-627.
Sugawara, M.,
Suzuki, K., Endo, K., Kumemura, M., Takeuchi, M., and Mitsuoka, T. (1990). Effect of the dietary supplementation of corn hemicellulose on fecal flora and
bacterial enzyme activities in human adults. Agricultural
and Biological Chemistry. 54(7): 1683-1688.
Swennen, K.,
Courtin, C. M., Lindemans, G. C. J. E., and Delcour, J. A. (2006). Large-scale production and characterisation of wheat bran arabinoxylooligosac-charides. Journal of the Science of Food and Agriculture. 86(11):
1722-1731.
Tissier, H.
(1900). Recherches sur la flora intestinale des nourrissons. Faculté de
médecine. Paris, France: Dissertation. 253 Pp.
Tong, L. T.,
Zhong, K., Liu, L., Qiu, J., Guo, L., Zhou, X., Cao, L., and Zhou, S. (2014). Effects of dietary wheat bran
arabinoxylans on cholesterol metabolism
of hypercholesterolemic hamsters. Carbohydrate Polymers. 112: 1-5.
Topping, D. L. and
Clifton, P. M. (2001). Short-chain fatty
acids and human colonic function: roles of resistant starch and nonstarch polysaccharides.Physiological Reviews. 81(3): 1031-1064.
Van-Craeyveld, V.,
Swennen, K., Dornez, E., Van-de-Wiele, T., Marzorati, M., Verstraete, W., …,
and Courtin, C. M. (2008). Structurally
different wheat-derived arabinoxylooligosaccharides have different
prebiotic and fermentation properties in rats. Journal of
Nutrition. 138(12): 2348-2355.
Van-den-Abbeele,
P., Gérard, P., Rabot, S., Bruneau, A., El-Aidy, S., Derrien, M., …, and
Possemiers, S. (2011). Arabinoxylans and inulin differentially modulate the
mucosal and luminal gut microbiota and mucin-degradation in humanized rats. Environmental
Microbiology. 13(10): 2667-2680.
Van-den-Ende, W.,
Peshev, D., and De-Gara, L. (2011). Disease prevention by natural antioxidants and
prebiotics acting as ROS scavengers in the gastrointestinal tract. Trends in Food Science & Technology. 22(12): 689-697.
Vardakou, M., Palop, C. N., Christakopoulos, P., Faulds, C. B., Gasson, M.
A., and Narbad, A. (2008). Evaluation of the prebiotic properties of wheat
arabinoxylan fractions and induction of hydrolase activity in gut microflora. International
Journal of Food Microbiology. 123(1): 166-170.
Veillon, A. and
Zuber, A. (1898). Recherches sur quelques microbes strictment anakrobies et
leur role en pathologie. Archives de Médicine Expérimentale d
‘Anatomie Pathologique. 10: 517-545.
Veenashri, B. R.
and Muralikrishna, G. (2011). In vitro anti-oxidant activity of xylo-oligosaccharides
derived from cereal and millet brans – A comparative study. Food
Chemistry. 126(3): 1475-1481.
Vogel, B.,
Gallaher, D. D., and Bunzel, M. (2012). Influence of cross-linked arabinoxylans
on the post-prandial blood glucose response in rats. Journal of
Agricultural and Food
Chemistry. 60(15): 3847-3852.
Wallace, B. D.,
Roberts, A. B., Pollet, R. M., Ingle, J. D., Biernat, K. A., Pellock, S. J., …,
and Dollinger, M. (2015). Structure and Inhibition of Microbiome β-Glucuronidases
Essential to the Alleviation of Cancer Drug Toxicity. Chemistry &
Biology. 22(9): 1238–1249.
Walton, G. E., Lu,
C., Trogh, I., Arnaut, F., and Gibson, G. R. (2012). A ramdomised,
double-blind, placebo controlled cross-over study to determine the gastrointestinal
effects of consumption of arabinoxylan-oligosaccharides enriched bread in
healthy volunteers. Nutrition Journal. 11(1): 36.
Wang, P., Tao, H.,
Jin, Z., and Xu, X. (2016). Impact of water extractable arabinoxylan from rye
bran on the frozen steamed bread dough quality. Food
Chemistry. 200: 117-124.
WHO, World Health
Organization (2017). World Health Statistics 2017: Monitoring
health for the SDGs: sustainable development goals. [En linea]. Disponible en:
www.int/gho/publications/world_helath_statistics/2017/en/. Fecha de consulta:
16 de enero de 2018.
Williams,
B. A., Zhang, D., Lisle, A. T., Mikkelsen, D., McSwe, C. S., Kang, S., …, and
Gidley, M. J. (2016). Soluble arabinoxylan enhances large intestinal microbial health
biomarkers in pigs fed a red meatcontaining diet. Nutrition. 32(4): 491-497.
Yacoubi, N.,
Van-Immerseel, F., Ducatelle, R., Rhayat, L., Bonnin, E., and Saulnier, L.
(2016). Water-soluble fractions obtained by enzymatic treatment of wheat grains
promote short chain fatty acids production by
broiler cecal microbiota. Animal Feed
Science and Technology. 218: 110-119.
Yadav, M. P. and
Hicks, K. B. (2018, en prensa). Isolation, characterization and functionalities
of biofiber gums isolated from grain processing by-products, agricultural
residues and energy crops. Food Hydrocolloids. DOI: 10.1016/j.foodhyd.2017.04.009.
Yadav, M. P.,
Kale, M. S., Hicks, K. B., and Hanah, K. (2017). Isolation, characterization
and the functional properties of cellulosic
arabinoxylan fiber isolated from agricultural processing by-products,
agricultural residues and energy crops. Food
Hydrocolloids. 63: 545-551.
Zhang, Z., Smith, C. J., Li, W., and Ashworth, J. (2016).
Characterization of nitric oxide modulatory activities
of alkaline-extracted and enzymaticmodified arabinoxylans
from corn bran in cultured human monocytes. Journal of Agricultural and Food Chemistry. 64(43): 8129-8137.
Zhang, D., Williams, B. A., Mikkelsen, D., Li, X., Keates, H. L., Lisle, A.
T., …, and Gidley, M. J. (2015). Soluble arabinoxylan alters digesta flow and protein digestion of red meat-containing diets
in pigs. Nutrition. 31(9): 1141-1147.
Zhou, S., Liu, X.,
Guo, Y., Wang, Q., Peng, D., and Cao, L. (2010). Comparison of the
immunological activities of arabinoxylans from wheat bran with alkali and xylanase-aided extraction. Carbohydrate Polymers. 81(4): 784-789.